Nové publikácie
Vedci sledujú prvé fyzické zmeny v bunkách, ktoré spôsobujú rakovinu
Posledná kontrola: 02.07.2025

Všetok obsah iLive je lekársky kontrolovaný alebo kontrolovaný, aby sa zabezpečila čo najväčšia presnosť faktov.
Máme prísne smernice týkajúce sa získavania zdrojov a len odkaz na seriózne mediálne stránky, akademické výskumné inštitúcie a vždy, keď je to možné, na lekársky partnerské štúdie. Všimnite si, že čísla v zátvorkách ([1], [2] atď.) Sú odkazmi na kliknutia na tieto štúdie.
Ak máte pocit, že niektorý z našich obsahov je nepresný, neaktuálny alebo inak sporný, vyberte ho a stlačte kláves Ctrl + Enter.
Keď je rakovina diagnostikovaná, na bunkovej a molekulárnej úrovni už prebieha mnoho udalostí, ktoré si ľudia nevšimli. Hoci sa rakovina pre klinické účely klasifikuje na skoré a neskoré štádiá, aj nádor v „skorom“ štádiu je výsledkom mnohých predchádzajúcich zmien v tele, ktoré boli nezistiteľné.
Vedci z Lekárskej fakulty Yaleovej univerzity (YSM) a ich kolegovia teraz získali podrobný prehľad o niektorých z týchto skorých zmien pomocou výkonnej mikroskopie s vysokým rozlíšením na sledovanie prvých fyzikálnych zmien spôsobujúcich rakovinu v kožných bunkách myší.
Štúdiom myší s mutáciou, ktorá podporuje rakovinu vlasových folikulov, vedci zistili, že prvé príznaky vzniku rakoviny sa vyskytujú v konkrétnom čase a na určitom mieste rastu vlasových folikulov myší. Navyše zistili, že tieto prekancerózne zmeny možno blokovať liekmi známymi ako inhibítory MEK.
Tím viedol Tianchi Xin, PhD, výskumný pracovník na Katedre genetiky YSM, a jeho súčasťou boli aj Valentina Greco, PhD, profesorka genetiky na YSM a členka Yale Cancer Center a Yale Stem Cell Center, a Sergi Regot, PhD, docent molekulárnej biológie a genetiky na Johns Hopkins School of Medicine.
Výsledky ich výskumu boli publikované v časopise Nature Cell Biology.
Vedci skúmali myši, u ktorých sa vyvinul spinocelulárny karcinóm kože, druhý najčastejší typ rakoviny kože u ľudí. Tieto myši boli geneticky modifikované mutáciou v géne KRAS, ktorý podporuje rakovinu a je jedným z najčastejšie mutovaných onkogénov v ľudských rakovinách. Mutácie KRAS sa zistili aj pri rakovine pľúc, pankreasu a hrubého čreva a konečníka.
Medzi skoré zmeny, ktoré vedci skúmali, patril rast drobnej, abnormálnej hrčky vo vlasovom folikule, ktorá je klasifikovaná ako prekancerózna abnormalita. „Pochopenie týchto skorých udalostí nám môže pomôcť vyvinúť prístupy k prevencii vzniku rakoviny,“ povedal Xin, hlavný autor štúdie.
Hoci sa ich štúdia zameriava na rakovinu kože, výskumníci sa domnievajú, že princípy, ktoré objavili, by sa dali aplikovať aj na mnoho iných druhov rakoviny spôsobených mutáciami KRAS, pretože kľúčové gény a proteíny zapojené do týchto procesov sú rovnaké vo všetkých nádoroch.
Viac než len proliferácia buniek U ľudí aj myší vlasové folikuly neustále rastú, strácajú staré vlasy a tvoria nové. Kmeňové bunky, ktoré majú schopnosť vyvinúť sa do rôznych typov buniek, zohrávajú v tomto procese obnovy veľkú úlohu. Predchádzajúce štúdie ukázali, že mutácie KRAS vedú k zvýšenej proliferácii kmeňových buniek vo vlasových folikuloch a tento veľký nárast kmeňových buniek bol považovaný za zodpovedný za prekancerózne ochorenie tkaniva.
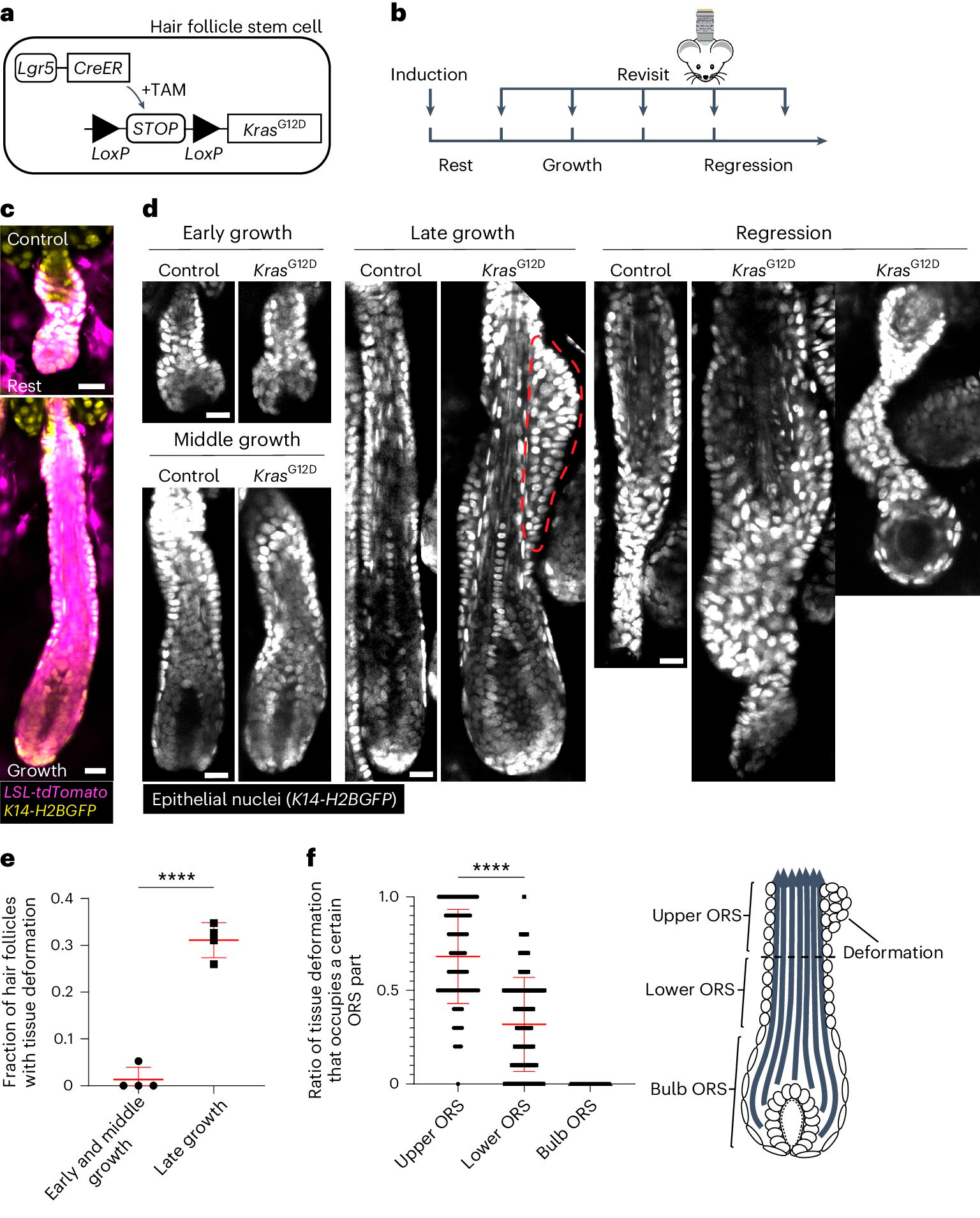
KrasG12D indukuje špecifické priestorovo-časové deformácie tkaniva počas regenerácie vlasových folikulov.
A. Schéma genetického prístupu k indukcii KrasG12D v kmeňových bunkách vlasových folikulov pomocou tamoxifénom indukovateľného systému Cre-LoxP (TAM).
B. Schéma znázorňujúca načasovanie indukcie KrasG12D a opätovného zobrazovania v porovnaní so štádiami vlasového cyklu.
C. Reprezentatívne snímky kľudových a rastúcich vlasových folikulov divokého typu obsahujúcich Cre-indukovateľný reportér tdTomato (Magenta) po indukcii.
D. Reprezentatívne snímky kontrolných a vlasových folikulov KrasG12D v rôznych štádiách vlasového cyklu. Deformácia tkaniva ako tuberkuly vo vonkajšom koreňovom puzdre (ORS) je znázornená červenou bodkovanou čiarou.
E. Podiel vlasových folikulov KrasG12D s deformáciou tkaniva v rôznych štádiách rastu vlasových folikulov.
F. Podiel deformácií tkaniva zaberajúcich hornú, dolnú a cibuľovitú časť ORS pre jednotlivé vlasové folikuly KrasG12D.
Zdroj: Nature Cell Biology (2024). DOI: 10.1038/s41556-024-01413-y
Na overenie tejto myšlienky tím použil špeciálne vytvorenú formu mutovaného KRAS, ktorú dokázali aktivovať v určitých časoch v kožných bunkách vlasových folikulov zvierat. Xin a jeho kolegovia použili mikroskopickú techniku známu ako intravitálne zobrazovanie, ktorá umožňuje snímanie buniek s vysokým rozlíšením in vivo a označovanie a sledovanie jednotlivých kmeňových buniek u zvierat.
Keď sa aktivovala mutácia KRAS, všetky kmeňové bunky sa začali množiť rýchlejšie, ale prekancerózna hrčka sa vytvorila iba na jednom konkrétnom mieste vo vlasovom folikule a v jednom štádiu rastu, čo znamená, že celkový nárast počtu buniek pravdepodobne nebol celým príbehom.
Aktivácia mutácie KRAS vo vlasových folikuloch viedla k rýchlejšej proliferácii kmeňových buniek, zmene ich migračných vzorcov a deleniu sa v rôznych smeroch v porovnaní s bunkami bez mutácie podporujúcej rakovinu.
Mutácia ovplyvňuje proteín známy ako ERK. Spoločnosť Xin dokázala monitorovať aktivitu ERK v reálnom čase v jednotlivých kmeňových bunkách živých zvierat a zistila špecifickú zmenu v aktivite tohto proteínu spôsobenú mutáciou KRAS. Výskumníci tiež dokázali zastaviť tvorbu prekanceróznej hrčky pomocou inhibítora MEK, ktorý blokuje aktivitu ERK.
Liek zastavil účinky mutácie na migráciu a orientáciu buniek, ale nie na celkovú proliferáciu kmeňových buniek, čo znamená, že vznik prekancerózneho stavu je spôsobený týmito prvými dvoma zmenami, a nie zvýšenou proliferáciou buniek.
Prekancerózne zmeny v kontexte Sledovanie účinkov onkogénnej mutácie v reálnom čase v živom organizme je jediný spôsob, akým výskumníci dokázali odhaliť tieto princípy. Je to dôležité, pretože rakovina sa netvorí vo vákuu – jej rast a udržiavanie je vo veľkej miere závislé od svojho mikroprostredia. Vedci tiež potrebovali sledovať nielen správanie jednotlivých buniek, ale aj molekuly vo vnútri týchto buniek.
„Prístup, ktorý sme zvolili k pochopeniu týchto onkogénnych udalostí, je v skutočnosti o prepojení naprieč úrovňou,“ povedal Greco. „Štruktúra a prístupy, ktoré použili Dr. Xin a Dr. Regot, nám umožnili ísť až k molekulárnym prvkom, prepojiť ich s bunkovou a tkanivovou úrovňou, čo nám poskytlo rozlíšenie týchto udalostí, ktoré je tak ťažké dosiahnuť mimo živého organizmu.“
Výskumníci teraz chcú sledovať proces počas dlhšieho časového obdobia, aby zistili, čo sa stane po vytvorení počiatočnej vydutiny. Chcú tiež študovať ďalšie onkogénne udalosti, ako je zápal, aby zistili, či sa objavené princípy dajú aplikovať aj v iných kontextoch.
