TIVDAK® Schválené FDA: Zacielenie na tkanivový faktor pri rakovine krčka maternice
Posledná kontrola: 14.06.2024

Všetok obsah iLive je lekársky kontrolovaný alebo kontrolovaný, aby sa zabezpečila čo najväčšia presnosť faktov.
Máme prísne smernice týkajúce sa získavania zdrojov a len odkaz na seriózne mediálne stránky, akademické výskumné inštitúcie a vždy, keď je to možné, na lekársky partnerské štúdie. Všimnite si, že čísla v zátvorkách ([1], [2] atď.) Sú odkazmi na kliknutia na tieto štúdie.
Ak máte pocit, že niektorý z našich obsahov je nepresný, neaktuálny alebo inak sporný, vyberte ho a stlačte kláves Ctrl + Enter.
Dňa 29. Apríla 2024 americký Úrad pre kontrolu potravín a liečiv (FDA) plne schválil TIVDAK® (tisotumab vedotin) od Seagen Inc., ktorý sa zameriava na tkanivový faktor (TF) na liečbu pacientok s rekurentným alebo metastatickým karcinómom krčka maternice, ktorí progredovali počas alebo po chemoterapia. To predstavuje významný prielom v terapii rakoviny krčka maternice, čo poukazuje na potenciál konjugátov protilátka-liek (ADC) v onkológii.
Mechanizmus účinku TIVDAK
Tivdak je liek ADC, ktorý sa zameriava na TF, ktorý kombinuje monoklonálnu protilátku proti TF tisotumab od spoločnosti Genmab s technológiou ADC od spoločnosti Seagen navrhnutou na zacielenie antigénov TF na rakovinové bunky a dodanie cytotoxickej skupiny MMAE priamo do rakovinových buniek. p>
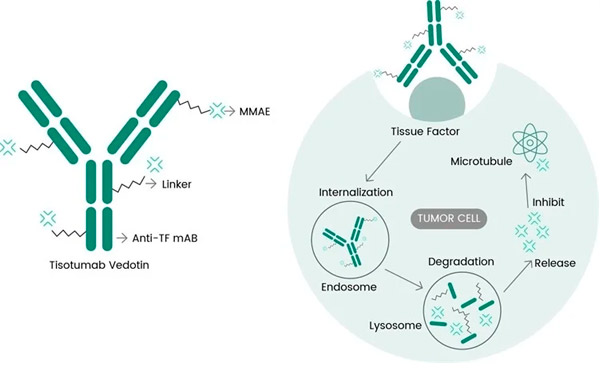
Молекулярный механизм действия тисотумаба ведотина (https://doi.org/10.3390/ijms23073559)
TF: идеальная мишень для разработки ADC
Известно, что TF участвует в сигнальных путях опухолевого роста и ангиогенереренере уется у подавляющего большинства пациентов с раком шейки матки и ххегих доруру Его способность ыстро интернализоваться при сзы ызызызызызывании и антитеvoľ ва крови дополнительно повышышт его п9одность для целенаправленой терапииака.
