Vedci identifikujú mutácie, ktoré chránia pred rakovinou B-buniek
Posledná kontrola: 14.06.2024

Všetok obsah iLive je lekársky kontrolovaný alebo kontrolovaný, aby sa zabezpečila čo najväčšia presnosť faktov.
Máme prísne smernice týkajúce sa získavania zdrojov a len odkaz na seriózne mediálne stránky, akademické výskumné inštitúcie a vždy, keď je to možné, na lekársky partnerské štúdie. Všimnite si, že čísla v zátvorkách ([1], [2] atď.) Sú odkazmi na kliknutia na tieto štúdie.
Ak máte pocit, že niektorý z našich obsahov je nepresný, neaktuálny alebo inak sporný, vyberte ho a stlačte kláves Ctrl + Enter.
Výskumníkom z University of Texas Southwestern Medical Center sa podarilo potlačiť leukémiu a lymfóm u myšacieho modelu geneticky predisponovaného na tieto druhy rakoviny úplným alebo čiastočným vyčerpaním proteínu nazývaného midnolín v B bunkách.
Ich zistenia, publikované v Journal of Experimental Medicine, by mohli viesť k vývoju nových liečebných postupov pre tieto choroby, ktoré by zabránili závažným vedľajším účinkom súčasných terapií.
„Na nájdenie cieľového lieku sme použili čisto genetickú metódu a tento cieľ sa ukázal byť senzačným, pretože B-bunkové leukémie a lymfómy sú od neho veľmi závislé, zatiaľ čo väčšina hostiteľských tkanív nie,“ povedal vedúci štúdie Bruce Beutler., MD, je riaditeľom Centra pre genetickú obranu hostiteľa a profesorom imunológie a internej medicíny na University of Texas Southwestern Medical Center.
Dr. Bütler, ktorý v roku 2011 získal Nobelovu cenu za fyziológiu a medicínu za objav dôležitej skupiny patogénnych senzorov známych ako Toll-like receptory nájdené na imunitných bunkách, dlho využíval mutagenézu – zavedenie mutácií do génov zvieracích modelov. Ich vystavenie chemikáliám. Látka nazývaná N-etyl-N-nitrózomočovina (ENU) ako kľúčový nástroj na štúdium funkcie génu.
Beutlerovo laboratórium nedávno vyvinulo metódu známu ako automatizované meiotické mapovanie (AMM), ktorá sleduje nezvyčajné znaky u mutantných myší späť k kauzálnym mutáciám, čím identifikuje gény nevyhnutné na udržanie normálnej fyziológie.
Mutagenéza často spôsobuje vývoj genetických chorôb u zvierat, čo poskytuje pohľad na funkciu postihnutých génov štúdiom abnormalít u zvierat. Ako však vysvetlil doktor Beutler, mutácie môžu tiež poskytnúť ochranu pred chorobami.
Príklady zahŕňajú mutácie, ktoré chránia ľudí s HIV alebo ľudí s dedičnou kosáčikovitou anémiou pred rozvojom symptómov. Mechanizmy, ktoré sú základom niektorých ochranných mutácií, inšpirovali vývoj liekov na liečbu rôznych chorôb.
Pri hľadaní ochranných mutácií pre poruchy imunity výskumníci testovali mutantné myši na imunitné bunky s neobvyklými vlastnosťami. U niekoľkých skupín zvierat s nezvyčajne nízkym počtom B buniek – dôležitej zložky adaptívneho imunitného systému zodpovedného za produkciu protilátok – výskumníci použili AMM na vysledovanie tohto nedostatku k mutáciám v mynolíne, proteíne, ktorý sa nachádza predovšetkým v B bunkách.
Hoci zvieratá, ktorým úplne chýba midnolín, umierajú počas vývoja pred narodením, miernejšie mutácie, vrátane niektorých zavedených genetickými technikami, ktoré odstránia gén v dospelosti, nespôsobili žiadne zjavné poškodenie.
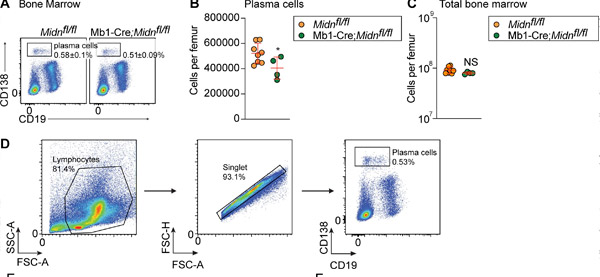
Produkcia plazmatických buniek po imunizácii TD antigénom β-galaktozidázou u myší Mb1-Cre; Midn fl/fl. (A a B) Reprezentatívne grafy prietokovej cytometrie (A) a počtu (B) plazmatických buniek v kostnej dreni 8-týždňových myší Mb1-Cre; Midn fl/fl a Midn fl/fl myší po imunizácii β- galaktozidáza. (C) Celkový počet buniek kostnej drene na femur. (D) Stratégia izolácie plazmatických buniek. Zdroj: Journal of Experimental Medicine (2024). DOI: 10.1084/jem.20232132
Výskumníci významne znížili alebo eliminovali midnolín u myší s genetickou predispozíciou na B-bunkové leukémie a lymfómy, rakoviny, pri ktorých sa B bunky nekontrolovateľne delia. Hoci myši s normálnymi hladinami stredovej línie zomreli na tieto choroby do 5 mesiacov, u väčšiny z tých, ktoré mali nižšiu alebo žiadnu strednú líniu, sa nikdy nevyvinuli zhubné nádory.
Ďalšie experimenty ukázali, že úlohou midnolínu v B bunkách je stimulovať aktivitu proteazómov, bunkových organel, ktoré recyklujú poškodené alebo už nepotrebné proteíny. Niektoré terapie, ktoré sa v súčasnosti používajú na liečbu B-bunkových leukémií a lymfómov, fungujú tak, že inhibujú aktivitu proteazómu, podobne ako odstránenie strednolínov, vysvetlil Dr. Beutler.
Avšak na rozdiel od týchto liekov, ktoré majú veľa potenciálne závažných vedľajších účinkov, eliminácia alebo redukcia midnolínu na zvieracích modeloch sa nezdá mať negatívne dôsledky.
Budúci výskum sa zameria na vývoj liekov, ktoré inhibujú midnolín, čo by v konečnom dôsledku mohlo poskytnúť základ pre novú liečbu rakoviny B-buniek.
