Lekársky expert článku
Nové publikácie
Corynebacterium
Posledná kontrola: 06.07.2025

Všetok obsah iLive je lekársky kontrolovaný alebo kontrolovaný, aby sa zabezpečila čo najväčšia presnosť faktov.
Máme prísne smernice týkajúce sa získavania zdrojov a len odkaz na seriózne mediálne stránky, akademické výskumné inštitúcie a vždy, keď je to možné, na lekársky partnerské štúdie. Všimnite si, že čísla v zátvorkách ([1], [2] atď.) Sú odkazmi na kliknutia na tieto štúdie.
Ak máte pocit, že niektorý z našich obsahov je nepresný, neaktuálny alebo inak sporný, vyberte ho a stlačte kláves Ctrl + Enter.
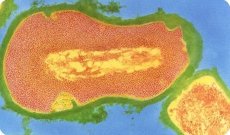
Záškrt je akútne infekčné ochorenie, postihujúce najmä deti, ktoré sa prejavuje ako hlboká intoxikácia tela difterickým toxínom a charakteristickým fibrinóznym zápalom v mieste lokalizácie patogénu. Názov ochorenia pochádza z gréckeho slova difthera - koža, film, pretože v mieste rozmnožovania patogénu sa tvorí hustý, sivobiely film.
Pôvodcu záškrtu - Corynebacterium diphtheriae - prvýkrát objavil v roku 1883 E. Klebs v rezoch filmu a v čistej kultúre ho získal v roku 1884 F. Leffler. V roku 1888 E. Roux a A. Yersin objavili jeho schopnosť produkovať exotoxín, ktorý hrá hlavnú úlohu v etiológii a patogenéze záškrtu. Výroba antitoxického séra E. Behringom v roku 1892 a jeho používanie od roku 1894 na liečbu záškrtu umožnilo výrazne znížiť úmrtnosť. Úspešný útok na toto ochorenie sa začal po roku 1923 v súvislosti s vývojom metódy na získanie záškrtového anatoxínu G. Raionom.
Pôvodca záškrtu patrí do rodu Corynebacterium (trieda Actinobacteria). Morfologicky sa vyznačuje tým, že bunky majú kyjovitý tvar a sú na koncoch zhrubnuté (grécky coryne - kyj), tvoria vetvičky, najmä v starých kultúrach, a obsahujú zrnité inklúzie.
Rod Corynebacterium zahŕňa veľké množstvo druhov, ktoré sú rozdelené do troch skupín.
- Korynebaktérie sú parazity ľudí a zvierat a sú pre ne patogénne.
- Korynebaktérie patogénne pre rastliny.
- Nepatogénne korynebaktérie. Mnohé druhy korynebaktérií sú bežnými obyvateľmi kože, slizníc hltana, nosohltana, očí, dýchacích ciest, močovej rúry a pohlavných orgánov.
Morfológia korynebaktérií
C. diphtheriae sú rovné alebo mierne zakrivené nepohyblivé tyčinky s dĺžkou 1,0 – 8,0 μm a priemerom 0,3 – 0,8 μm; netvoria spóry ani kapsuly. Často majú na jednom alebo oboch koncoch zdureniny a často obsahujú metachromatické granule – volutínové zrná (polymetafosfáty), ktoré po zafarbení metylénovou modrou získavajú modrofialové sfarbenie. Na ich detekciu bola navrhnutá špeciálna Neisserova farbiaca metóda. V tomto prípade sú tyčinky zafarbené slamovožlto a volutínové zrná sú tmavohnedé a zvyčajne sa nachádzajú na póloch. Corynebacterium diphtheriae sa dobre farbí anilínovými farbivami, je grampozitívna, ale v starých kultúrach sa často mení farbivom a má negatívne farbenie podľa Grama. Vyznačuje sa výrazným polymorfizmom, najmä v starých kultúrach a pod vplyvom antibiotík. Obsah G + C v DNA je približne 60 mol %.
Biochemické vlastnosti korynebaktérií
Bacil záškrtu je aerób alebo fakultatívne anaerób, teplotné optimum pre rast je 35 – 37 °C (limity rastu sú 15 – 40 °C), optimálne pH je 7,6 – 7,8. Nie je veľmi náročný na živné médiá, ale lepšie rastie na médiách obsahujúcich sérum alebo krv. Pre baktérie záškrtu sú selektívne Rouxove alebo Loefflerove médiá so zrazeným sérom, rast na nich sa objavuje po 8 – 12 hodinách vo forme konvexných kolónií veľkosti špendlíkovej hlavičky, sivobielej alebo žltkasto-krémovej farby. Ich povrch je hladký alebo mierne zrnitý, na obvode sú kolónie o niečo priehľadnejšie ako v strede. Kolónie sa nespájajú, v dôsledku čoho kultúra nadobúda vzhľad shagreenovej kože. Na bujóne sa rast prejavuje ako rovnomerný zákal, alebo bujón zostáva priehľadný a na jeho povrchu sa tvorí jemný film, ktorý postupne hustne, drobí sa a usadzuje sa vo vločkách na dne.
Charakteristickým znakom baktérií záškrtu je ich dobrý rast na krvných a sérových médiách obsahujúcich také koncentrácie teluritu draselného, že potláčajú rast iných typov baktérií. Je to spôsobené tým, že C. diphtheriae redukuje telurit draselný na kovový telúr, ktorý po usadení v mikrobiálnych bunkách dodáva kolóniám charakteristickú tmavosivú alebo čiernu farbu. Použitie takýchto médií zvyšuje percento očkovania baktérií záškrtu.
Corynebacterium diphtheriae fermentuje glukózu, maltózu, galaktózu za vzniku kyseliny bez plynov, ale nefermentuje (spravidla) sacharózu, má cystinázu, nemá ureázu a netvorí indol. Podľa týchto charakteristík sa líši od tých koryneformných baktérií (difteroidov), ktoré sa najčastejšie nachádzajú na sliznici oka (Corynebacterium xerosus) a nosohltana (Corynebacterium pseiidodiphtheriticum) a od ostatných difteroidov.
V prírode existujú tri hlavné varianty (biotypy) záškrtového bacilu: gravis, intermedins a mitis. Líšia sa morfologickými, kultúrnymi, biochemickými a inými vlastnosťami.
Rozdelenie baktérií záškrtu na biotypy bolo vykonané s ohľadom na formy záškrtu, u ktorých sú izolované s najväčšou frekvenciou. Typ gravis sa najčastejšie izoluje u pacientov s ťažkou formou záškrtu a spôsobuje skupinové ohniská. Typ mitis spôsobuje miernejšie a sporadické prípady ochorenia a typ intermedius zaujíma medzi nimi medziľahlú pozíciu. Corynebacterium belfanti, predtým pripisovaný biotypu mitis, je izolovaný ako nezávislý, štvrtý biotyp. Jeho hlavný rozdiel od biotypov gravis a mitis je schopnosť redukovať dusičnany na dusitany. Kmene Corynebacterium belfanti majú výrazné adhezívne vlastnosti a nachádzajú sa medzi nimi toxigénne aj netoxigénne varianty.
 [ 6 ], [ 7 ], [ 8 ], [ 9 ], [ 10 ]
[ 6 ], [ 7 ], [ 8 ], [ 9 ], [ 10 ]
Antigénna štruktúra korynebaktérií
Corynebacterium je veľmi heterogénne a mozaikové. Vo všetkých troch typoch patogénov záškrtu sa našlo niekoľko desiatok somatických antigénov, podľa ktorých sa delia na sérotypy. V Rusku bola prijatá sérologická klasifikácia, podľa ktorej sa rozlišuje 11 sérotypov baktérií záškrtu, z ktorých 7 je hlavných (1-7) a 4 sú doplnkové, zriedkavo sa vyskytujúce sérotypy (8-11). Šesť sérotypov (1, 2, 3, 4, 5, 7) patrí do typu gravis a päť (6, 8, 9, 10, 11) patrí do typu mitis. Nevýhodou metódy sérotypizácie je, že mnohé kmene, najmä netoxigénne, majú spontánnu aglutináciu alebo polyaglutinabilitu.
 [ 11 ]
[ 11 ]
Fágová typizácia Corynebacterium diphtheriae
Na diferenciáciu baktérií záškrtu boli navrhnuté rôzne schémy fágovej typizácie. Podľa schémy M. D. Krylova je možné pomocou súboru 9 fágov (A, B, C, D, F, G, H, I, K) typovať väčšinu toxigénnych a netoxigénnych kmeňov typu gravis. S ohľadom na citlivosť na špecifikované fágy, ako aj na kultúrne, antigénne vlastnosti a schopnosť syntetizovať korycíny (baktericídne proteíny), M. D. Krylova identifikovala 3 nezávislé skupiny korynebaktérií typu gravis (I-III). Každá z nich obsahuje podskupiny toxigénnych a ich netoxigénne analógy patogénov záškrtu.
Rezistencia voči korynebaktériám
Corynebacterium diphtheriae vykazuje vysokú odolnosť voči nízkym teplotám, ale pri vysokých teplotách rýchlo hynie: pri 60 °C - do 15-20 minút, pri vare - po 2-3 minútach. Všetky dezinfekčné prostriedky (lyzol, fenol, chlóramín atď.) v bežne používanej koncentrácii ho ničia za 5-10 minút. Patogén záškrtu však dobre znáša sušenie a môže dlhodobo zostať životaschopný v vysušenom hliene, slinách a prachových časticiach. V jemnom aerosóle zostávajú baktérie záškrtu životaschopné 24-48 hodín.
Faktory patogenity korynebaktérií
Patogenita Corynebacterium diphtheriae je určená prítomnosťou viacerých faktorov.
Faktory adhézie, kolonizácie a invázie
Štruktúry zodpovedné za adhéziu neboli identifikované, ale bez nich by difterický bacil nebol schopný kolonizovať bunky. Ich úlohu plnia niektoré zložky bunkovej steny patogénu. Invazívne vlastnosti patogénu sú spojené s hyaluronidázou, neuraminidázou a proteázou.
Toxický glykolipid obsiahnutý v bunkovej stene patogénu. Je to 6,6'-diester trehalózy obsahujúci kyselinu korynemykolovú (C32H64O3) a kyselinu korynemykolovú (C32H62O3) v ekvimolárnych pomeroch (trehalóza-6,6'-dikorynemikolát). Glykolipid má deštruktívny účinok na tkanivové bunky v mieste rozmnožovania patogénu.
Exotoxín, ktorý určuje patogenitu patogénu a povahu patogenézy ochorenia. Netoxigénne varianty C. diphtheriae nespôsobujú záškrt.
Exotoxín sa syntetizuje ako neaktívny prekurzor - jeden polypeptidový reťazec s molekulovou hmotnosťou 61 kD. Aktivuje ho samotná bakteriálna proteáza, ktorá štiepi polypeptid na dva peptidy spojené disulfidovými väzbami: A (mw 21 kD) a B (mw 39 kD). Peptid B plní akceptorovú funkciu - rozpoznáva receptor, viaže sa naň a tvorí intramembránový kanál, cez ktorý peptid A preniká do bunky a realizuje biologickú aktivitu toxínu. Peptid A je enzým ADP-ribozyltransferáza, ktorý zabezpečuje prenos adenozíndifosfátribózy z NAD na jeden z aminokyselinových zvyškov (histidín) elongačného faktora proteínu EF-2. V dôsledku modifikácie EF-2 stráca svoju aktivitu, čo vedie k potlačeniu syntézy proteínov ribozómami v štádiu translokácie. Toxín syntetizujú iba tie C. diphtheriae, ktoré nesú vo svojom chromozóme gény mierneho konvertujúceho profága. Operón kódujúci syntézu toxínu je monocistronický, pozostáva z 1,9 tisíca nukleotidových párov a má promótor toxP a 3 oblasti: toxS, toxA a toxB. Oblasť toxS kóduje 25 aminokyselinových zvyškov signálneho peptidu (zabezpečuje uvoľňovanie toxínu cez membránu do periplazmatického priestoru bakteriálnej bunky), toxA - 193 aminokyselinových zvyškov peptidu A a toxB - 342 aminokyselinových zvyškov peptidu B toxínu. Strata profágu bunkou alebo mutácie v tox operóne robia bunku mierne toxigénnou. Naopak, lyzogenizácia netoxigénnych C. diphtheriae konvertujúcim fágom ich mení na toxigénne baktérie. Toto bolo jednoznačne dokázané: toxigénnosť difterických baktérií závisí od ich lyzogenizácie tox-konvertujúcimi korynefágmi. Korynefágy sa integrujú do chromozómu korynebaktérií pomocou mechanizmu miestne špecifickej rekombinácie a kmene baktérií záškrtu môžu obsahovať vo svojich chromozómoch 2 rekombinačné miesta (attB) a korynefágy sa integrujú do každého z nich s rovnakou frekvenciou.
Genetická analýza viacerých netoxigénnych kmeňov baktérií záškrtu, vykonaná pomocou značených DNA sond nesúcich fragmenty korynefágového tox operónu, ukázala, že ich chromozómy obsahujú sekvencie DNA homológne s korynefágovým tox operónom, ale buď kódujú neaktívne polypeptidy, alebo sú v „tichom“ stave, t. j. neaktívne. V tejto súvislosti vyvstáva veľmi dôležitá epidemiologická otázka: môžu sa netoxigénne baktérie záškrtu v prirodzených podmienkach (v ľudskom tele) transformovať na toxigénne, podobne ako sa to deje in vitro? Možnosť takejto transformácie netoxigénnych kultúr korynebaktérií na toxigénne pomocou fágovej konverzie bola preukázaná v experimentoch na morčatách, kuracích embryách a bielych myšiach. Či sa to však deje počas prirodzeného epidemického procesu (a ak áno, ako často), zatiaľ nebolo stanovené.
Vzhľadom na to, že difterický toxín v tele pacientov má selektívny a špecifický účinok na určité systémy (postihnutý je najmä sympaticko-adrenálny systém, srdce, cievy a periférne nervy), je zrejmé, že nielenže inhibuje biosyntézu bielkovín v bunkách, ale spôsobuje aj ďalšie poruchy ich metabolizmu.
Na zistenie toxicity baktérií záškrtu možno použiť nasledujúce metódy:
- Biologické testy na zvieratách. Intradermálna infekcia morčiat filtrátom bujónovej kultúry difterických baktérií spôsobuje nekrózu v mieste vpichu. Jedna minimálna smrteľná dávka toxínu (20-30 ng) usmrtí morča s hmotnosťou 250 g pri subkutánnej injekcii na 4.-5. deň. Najcharakteristickejším prejavom účinku toxínu je poškodenie nadobličiek, ktoré sú zväčšené a prudko hyperemické.
- Infekcia kuracích embryí. Záškrtový toxín spôsobuje ich smrť.
- Infekcia bunkových kultúr. Difterický toxín spôsobuje výrazný cytopatický účinok.
- Test na pevnej fáze s enzýmovou imunosorbentnou analýzou s použitím antitoxínov značených peroxidázou.
- Použitie DNA sondy na priamu detekciu tox operónu v chromozóme baktérií záškrtu.
Najjednoduchšou a najbežnejšou metódou na stanovenie toxicity baktérií záškrtu je však sérologická - metóda gélovej precipitácie. Jej podstata je nasledovná. Pásik sterilného filtračného papiera s rozmermi 1,5 x 8 cm sa navlhčí antitoxickým antidifterickým sérom obsahujúcim 500 AE v 1 ml a nanesie sa na povrch živného média v Petriho miske. Miska sa suší v termostate 15-20 minút. Testovacie kultúry sa vysejú plakmi na oboch stranách papiera. Na jednu misku sa vyseje niekoľko kmeňov, z ktorých jeden, zjavne toxický, slúži ako kontrola. Misky s kultúrami sa inkubujú pri teplote 37 °C, výsledky sa berú do úvahy po 24-48 hodinách. V dôsledku protidifúzie antitoxínu a toxínu v géli sa v mieste ich interakcie vytvorí jasná precipitačná čiara, ktorá sa spája s precipitačnou čiarou kontrolného toxigénneho kmeňa. Nešpecifické precipitačné pásy (tvoria sa, ak sú okrem antitoxínu v sére prítomné v malom množstve aj iné antimikrobiálne protilátky) sa objavujú neskoro, sú slabo exprimované a nikdy sa nespájajú s precipitačným pásom kontrolného kmeňa.
Postinfekčná imunita
Silné, pretrvávajúce, prakticky celoživotné, opakované prípady ochorenia sa pozorujú zriedkavo - u 5-7 % tých, ktorí ochorenie prekonali. Imunita má prevažne antitoxický charakter, antimikrobiálne protilátky majú menší význam.
Schickov test sa predtým široko používal na posúdenie úrovne imunity proti záškrtu. Na tento účel sa deťom intradermálne injekčne podávala 1/40 morčacieho toxínu v objeme 0,2 ml. Pri absencii antitoxickej imunity sa v mieste vpichu po 24 – 48 hodinách objaví začervenanie a opuch s priemerom väčším ako 1 cm. Takáto pozitívna Schickova reakcia naznačuje buď úplnú absenciu antitoxínu, alebo jeho obsah je menší ako 0,001 AE/ml krvi. Negatívna Schickova reakcia sa pozoruje, keď je obsah antitoxínu v krvi vyšší ako 0,03 AE/ml. Ak je obsah antitoxínu nižší ako 0,03 AE/ml, ale vyšší ako 0,001 AE/ml, Schickova reakcia môže byť buď pozitívna, alebo niekedy negatívna. Okrem toho má samotný toxín výraznú alergénnu vlastnosť. Preto je na stanovenie úrovne imunity proti záškrtu (kvantitatívny obsah antitoxínu) lepšie použiť RPGA s diagnostickým erytrocytom senzibilizovaným záškrtovým toxoidom.
Epidemiológia záškrtu
Jediným zdrojom infekcie je človek – chorý, zotavujúci sa alebo zdravý nosič baktérií. K infekcii dochádza prostredníctvom kvapôčok vo vzduchu, prachu vo vzduchu a prostredníctvom rôznych predmetov, ktoré používajú chorí alebo zdraví nosiči: riad, knihy, bielizeň, hračky atď. V prípade kontaminácie potravín (mlieko, krémy atď.) je infekcia možná alimentárnou cestou. Najmasívnejšie vylučovanie patogénu nastáva pri akútnej forme ochorenia. Najväčší epidemiologický význam však majú ľudia s latentnými, atypickými formami ochorenia, pretože často nie sú hospitalizovaní a nie sú okamžite zistení. Pacient so záškrtom je infekčný počas celého obdobia ochorenia a časti obdobia zotavovania. Priemerné obdobie nosičstva baktérií u zotavujúcich sa ľudí sa pohybuje od 2 do 7 týždňov, ale môže trvať až 3 mesiace.
Zdraví nosiči zohrávajú v epidemiológii záškrtu osobitnú úlohu. V podmienkach sporadickej chorobnosti sú hlavnými distribútormi záškrtu, čo prispieva k zachovaniu patogénu v prírode. Priemerné trvanie nosičstva toxigénnych kmeňov je o niečo kratšie (približne 2 mesiace) ako netoxigénnych (približne 2-3 mesiace).
Dôvod vzniku zdravého nosičstva toxigénnych a netoxigénnych baktérií záškrtu nebol úplne odhalený, pretože ani vysoká úroveň antitoxickej imunity nie vždy zabezpečuje úplné oslobodenie tela od patogénu. Určitý význam má možno úroveň antibakteriálnej imunity. Primárny epidemiologický význam má nosičstvo toxigénnych kmeňov baktérií záškrtu.
 [ 12 ], [ 13 ], [ 14 ], [ 15 ], [ 16 ], [ 17 ], [ 18 ], [ 19 ]
[ 12 ], [ 13 ], [ 14 ], [ 15 ], [ 16 ], [ 17 ], [ 18 ], [ 19 ]
Príznaky záškrtu
Na záškrt sú náchylní ľudia v akomkoľvek veku. Patogén môže preniknúť do ľudského tela cez sliznice rôznych orgánov alebo cez poškodenú kožu. V závislosti od lokalizácie procesu sa rozlišuje záškrt hltana, nosa, hrtana, ucha, oka, genitálií a kože. Možné sú zmiešané formy, napríklad záškrt hltana a kože atď. Inkubačná doba je 2-10 dní. Pri klinicky prejavenej forme záškrtu sa v mieste lokalizácie patogénu vyvíja charakteristický fibrinózny zápal sliznice. Toxín produkovaný patogénom najprv ovplyvňuje epitelové bunky a potom blízke cievy, čím zvyšuje ich priepustnosť. Vychádzajúci exsudát obsahuje fibrinogén, ktorého koagulácia vedie k tvorbe sivobieleho filmového povlaku na povrchu sliznice, ktorý je pevne srastený s podkladovým tkanivom a po odtrhnutí spôsobuje krvácanie. Dôsledkom poškodenia ciev môže byť vznik lokálneho edému. Záškrt hltana je obzvlášť nebezpečný, pretože môže spôsobiť záškrtovú krupicu v dôsledku edému sliznice hrtana a hlasiviek, na ktorú predtým zomieralo 50 – 60 % detí so záškrtom v dôsledku asfyxie. Záškrtový toxín, ktorý sa dostáva do krvi, spôsobuje celkovú hlbokú intoxikáciu. Postihuje najmä kardiovaskulárny, sympaticko-adrenálny systém a periférne nervy. Príznaky záškrtu teda pozostávajú z kombinácie lokálnych príznakov v závislosti od lokalizácie vstupnej brány a všeobecných príznakov spôsobených otravou toxínom, ktoré sa prejavujú vo forme adynamie, letargie, bledej pokožky, nízkeho krvného tlaku, myokarditídy, paralýzy periférnych nervov a iných porúch. Záškrt u očkovaných detí, ak sa pozoruje, zvyčajne prebieha v miernej forme a bez komplikácií. Úmrtnosť v období pred použitím séroterapie a antibiotík bola 50 – 60 %, teraz je to 3 – 6 %.
Laboratórna diagnostika záškrtu
Jedinou metódou mikrobiologickej diagnostiky záškrtu je bakteriologická, s povinným testovaním izolovanej kultúry korynebaktérií na toxicitu. Bakteriologické štúdie na záškrt sa vykonávajú v troch prípadoch:
- na diagnostiku záškrtu u detí a dospelých s akútnymi zápalovými procesmi v hltane, nose a nosovej časti hltana;
- podľa epidemiologických indikácií osôb, ktoré boli v kontakte so zdrojom patogénu záškrtu;
- osoby novo prijaté do sirotincov, jaslí, internátnych škôl a iných špeciálnych zariadení pre deti a dospelých, s cieľom identifikovať medzi nimi možných nosičov záškrtu.
Materiálom na štúdiu je hlien z hltana a nosa, film z mandlí alebo iných slizníc, ktoré sú vstupným bodom pre patogén. Výsev sa vykonáva na teluritové sérum alebo krvné médiá a súčasne na koagulované sérové Roux (koagulované konské sérum) alebo Loefflerovo (3 diely hovädzieho séra + 1 diel cukrového vývaru) médiá, na ktorých sa rast korynebaktérií objaví po 8 – 12 hodinách. Izolovaná kultúra sa identifikuje kombináciou morfologických, kultivačných a biochemických vlastností, pričom sa vždy, keď je to možné, používajú metódy séro- a fágového typovania. Vo všetkých prípadoch je povinný test toxicity s použitím jednej z vyššie uvedených metód. Morfologické znaky korynebaktérií sa najlepšie študujú pomocou troch metód farbenia náteru: Gramovou, Neisserovou a metylénovou modrou (alebo toluidínovou modrou).
Liečba záškrtu
Špecifickou liečbou záškrtu je použitie antitoxického séra proti záškrtu s obsahom najmenej 2000 IU na 1 ml. Sérum sa podáva intramuskulárne v dávkach od 10 000 do 400 000 IU v závislosti od závažnosti ochorenia. Účinnou liečebnou metódou je použitie antibiotík (penicilíny, tetracyklíny, erytromycín atď.) a sulfónamidov. Na stimuláciu produkcie vlastných antitoxínov možno použiť anatoxín. Na odstránenie bakterionosiča by sa mali použiť antibiotiká, na ktoré je daný kmeň korynebaktérií vysoko citlivý.
Špecifická profylaxia záškrtu
Hlavnou metódou boja proti záškrtu je hromadné plánované očkovanie obyvateľstva. Na tento účel sa používajú rôzne možnosti vakcín vrátane kombinovaných, t. j. zameraných na súčasné vytvorenie imunity proti viacerým patogénom. Najrozšírenejšou vakcínou v Rusku je DPT. Ide o suspenziu baktérií čierneho kašľa adsorbovaných na hydroxid hlinitý, usmrtených formalínom alebo timerosalom (20 miliárd v 1 ml), ktorá obsahuje difterický toxoid v dávke 30 flokulačných jednotiek a 10 jednotiek viažucich tetanový toxoid v 1 ml. Deti sa očkujú od 3 mesiacov veku a potom sa vykonávajú revakcinácie: prvá po 1,5-2 rokoch, ďalšie vo veku 9 a 16 rokov a potom každých 10 rokov.
Vďaka hromadnému očkovaniu, ktoré sa v ZSSR začalo v roku 1959, sa výskyt záškrtu v krajine do roku 1966 v porovnaní s rokom 1958 znížil 45-krát a jeho ukazovateľ v roku 1969 bol 0,7 na 100 000 obyvateľov. Následné zníženie objemu očkovania v 80. rokoch 20. storočia viedlo k vážnym následkom. V rokoch 1993 – 1996 zasiahla Rusko epidémia záškrtu. Ochoreli dospelí, najmä tí, ktorí neboli očkovaní, a deti. V roku 1994 bolo zaregistrovaných takmer 40 tisíc pacientov. V súvislosti s tým sa obnovilo hromadné očkovanie. Počas tohto obdobia bolo zaočkovaných 132 miliónov ľudí, vrátane 92 miliónov dospelých. V rokoch 2000 – 2001 bola miera očkovania detí v stanovenom období 96 % a revakcináciou 94 %. Vďaka tomu sa výskyt záškrtu v roku 2001 v porovnaní s rokom 1996 znížil 15-násobne. Aby sa však výskyt znížil na ojedinelé prípady, je potrebné zaočkovať aspoň 97 – 98 % detí v prvom roku života a zabezpečiť hromadné preočkovanie v nasledujúcich rokoch. Je nepravdepodobné, že by sa záškrt v nasledujúcich rokoch úplne eliminoval kvôli rozsiahlemu prenášaniu toxigénnych a netoxigénnych baktérií záškrtu. Vyriešenie tohto problému si tiež vyžiada určitý čas.

