Lekársky expert článku
Nové publikácie
Netuberkulózne mykobaktérie
Posledná kontrola: 04.07.2025

Všetok obsah iLive je lekársky kontrolovaný alebo kontrolovaný, aby sa zabezpečila čo najväčšia presnosť faktov.
Máme prísne smernice týkajúce sa získavania zdrojov a len odkaz na seriózne mediálne stránky, akademické výskumné inštitúcie a vždy, keď je to možné, na lekársky partnerské štúdie. Všimnite si, že čísla v zátvorkách ([1], [2] atď.) Sú odkazmi na kliknutia na tieto štúdie.
Ak máte pocit, že niektorý z našich obsahov je nepresný, neaktuálny alebo inak sporný, vyberte ho a stlačte kláves Ctrl + Enter.
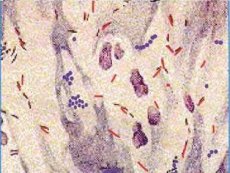
Netuberkulózne mykobaktérie sú samostatné druhy, rozšírené v prostredí ako saprofyty, ktoré v niektorých prípadoch môžu spôsobiť závažné ochorenia - mykobakteriózy. Nazývajú sa aj environmentálne mykobaktérie, pôvodcovia mykobakteriózy, oportúnne a atypické mykobaktérie. Významný rozdiel medzi netuberkulóznymi mykobaktériami a komplexom Mycobacterium tuberculosis spočíva v tom, že sa prakticky neprenášajú z človeka na človeka.
Netuberkulózne mykobaktérie sa delia do 4 skupín na základe obmedzeného počtu charakteristík: rýchlosť rastu, tvorba pigmentu, morfológia kolónií a biochemické vlastnosti.
1. skupina - pomaly rastúce fotochromogénne (M. kansasii atď.). Hlavným znakom zástupcov tejto skupiny je výskyt pigmentu na svetle. Tvoria kolónie od S do RS-formy, obsahujú kryštály karoténu, ktoré ich sfarbujú do žlta. Rýchlosť rastu je od 7 do 20 dní pri teplote 25, 37 a 40 °C, katadáza-pozitívne.
M. kansasii sú žlté bacily, ktoré žijú vo vode a pôde a najčastejšie postihujú pľúca. Tieto baktérie možno identifikovať podľa ich veľkej veľkosti a krížového usporiadania. Dôležitým prejavom infekcií spôsobených M. kansasii je rozvoj diseminovaného ochorenia. Možné sú aj lézie kože a mäkkých tkanív, rozvoj tenosynovitídy, osteomyelitídy, lymfadenitídy, perikarditídy a infekcií urogenitálneho traktu.
2. skupina - pomaly rastúce skotochromogénne (M. scrofulaceum, M. matmoense, M. gordonae atď.). Mikroorganizmy tvoria v tme žlté a na svetle oranžové alebo červenkasté kolónie, zvyčajne kolónie v tvare písmena S, rastú pri teplote 37 °C. Ide o najpočetnejšiu skupinu netuberkulóznych mykobaktérií. Sú izolované z kontaminovaných vodných plôch a pôdy a majú nízku patogénnosť pre ľudí a zvieratá.
M. scrofulaceum (z anglického scrofula - scrofula) je jednou z hlavných príčin cervikálnej lymfadenitídy u detí mladších ako 5 rokov. Pri závažných sprievodných ochoreniach môžu spôsobiť poškodenie pľúc, kostí a mäkkých tkanív. Okrem vody a pôdy boli mikróby izolované aj zo surového mlieka a iných mliečnych výrobkov.
M. maimoense sú mikroaerofily, ktoré tvoria sivobiele, hladké, lesklé, nepriehľadné, kupolovité, okrúhle kolónie.
Primárne izoláty rastú veľmi pomaly pri teplote 22 – 37 °C. Vystavenie svetlu nespôsobuje tvorbu pigmentu. V prípade potreby môže vystavenie pokračovať až 12 týždňov. U ľudí spôsobujú chronické ochorenie pľúc.
M. gordonae sú najčastejšie rozpoznané saprofyty, skotochromogény vody z vodovodu a spôsobujú mykobakteriózu extrémne zriedkavo. Okrem vody (známe ako M. aquae) sa často izolujú z pôdy, výplachu žalúdka, bronchiálnych sekrétov alebo iného materiálu od pacientov, ale vo väčšine prípadov sú pre ľudí nepatogénne. Zároveň existujú správy o prípadoch meningitídy, peritonitídy a kožných lézií spôsobených týmto typom mykobaktérií.
Skupina 3 - pomaly rastúce nechromogénne mykobaktérie (komplex M. avium, komplex M. gaslri, komplex M. terrae atď.). Tvoria bezfarebné S- alebo SR- a R-formy kolónií, ktoré môžu mať svetložlté a krémové odtiene. Izolujú sa z chorých zvierat, vody a pôdy.
M. avium - M. inlracellulare sú spojené do jedného komplexu M. avium, pretože ich medzidruhová diferenciácia predstavuje určité ťažkosti. Mikroorganizmy rastú pri teplote 25 – 45 °C, sú patogénne pre vtáky, menej patogénne pre hovädzí dobytok, ošípané, ovce, psy a nie sú patogénne pre morčatá. Najčastejšie tieto mikroorganizmy spôsobujú pľúcne lézie u ľudí. Boli opísané lézie kože, svalového tkaniva a kostry, ako aj diseminované formy ochorení. Patria medzi pôvodcov oportúnnych infekcií, ktoré komplikujú syndróm získanej imunodeficiencie (AIDS). Poddruh M. avium paratuberculosis je pôvodcom Jonesovej choroby u hovädzieho dobytka a pravdepodobne aj Crohnovej choroby (chronického zápalového ochorenia gastrointestinálneho traktu) u ľudí. Mikrób je prítomný v mäse, mlieku a výkaloch infikovaných kráv a nachádza sa aj vo vode a pôde. Štandardné metódy čistenia vody tento mikrób neinaktivujú.
M. xenopi spôsobuje u ľudí pľúcne lézie a diseminované formy ochorenia spojené s AIDS. Boli izolované zo žiab rodu Xenopus. Baktérie tvoria malé, hladké, lesklé, nepigmentované kolónie, ktoré následne zožltnú. Termofily nerastú pri teplote 22 °C a dobre rastú pri 37 a 45 °C. Pri bakterioskopickom vyšetrení vyzerajú ako veľmi tenké tyčinky, zužujúce sa na jednom konci a usporiadané rovnobežne vedľa seba (ako laťkový plot). Často sú izolované zo studenej a horúcej vody z vodovodu, vrátane pitnej vody uskladnenej v nemocničných zásobníkoch (nozokomiálne ohniská). Na rozdiel od iných oportúnnych mykobaktérií sú citlivé na väčšinu antituberkulóznych liekov.
M. ukerans je etiologickým pôvodcom mykobakteriálnej kožnej N (Buruliho vred), rastie iba pri teplote 30 – 33 °C, rast kolónií sa pozoruje až po 7 týždňoch. Patogén sa uvoľňuje aj pri infekcii myší v dreni chodidla labky. Toto ochorenie je bežné v Austrálii a Afrike. Zdrojom infekcie je tropické prostredie a BCG očkovanie proti tejto mykobakterióze.
Skupina 4 - rýchlo rastúce mykobaktérie (komplex M. fortuitum, M. phlei, M. xmegmatis atď.). Ich rast sa pozoruje vo forme kolónií v R- alebo S-forme počas 1-2 až 7 dní. Nachádzajú sa vo vode, pôde, odpadových vodách a sú zástupcami normálnej mikroflóry ľudského tela. Baktérie tejto skupiny sa zriedkavo izolujú z patologického materiálu od pacientov, ale niektoré z nich majú klinický význam.
Komplex M. fortuitum zahŕňa M. fortuitum a M. chcionae, ktoré pozostávajú z poddruhov. Spôsobujú diseminované procesy, kožné a pooperačné infekcie, ochorenia pľúc. Mikróby tohto komplexu sú vysoko rezistentné voči antituberkulóznym liekom.
M. smegmatis je zástupcom normálnej mikroflóry, izolovanej zo smegmy u mužov. Dobre rastie pri teplote 45 °C. Ako pôvodca ľudských ochorení sa radí na druhé miesto medzi rýchlo rastúcimi mykobaktériami po komplexe M. fortuitum. Postihuje kožu a mäkké tkanivá. Pri vyšetrení moču je potrebné odlíšiť patogény tuberkulózy od M. smegmatis.
Najčastejšie je mykobakterióza spôsobená zástupcami skupín 3 a 1.
Epidemiológia mykobakteriózy
Pôvodcovia mykobakteriózy sú v prírode rozšírení. Nachádzajú sa v pôde, prachu, rašeline, bahne, riečnej vode, rybníkoch a bazénoch. Nachádzajú sa v kliešťoch a rybách, spôsobujú choroby u vtákov, divých a domácich zvierat a sú zástupcami normálnej mikroflóry slizníc horných dýchacích ciest a urogenitálneho traktu u ľudí. Infekcia netuberkulóznymi mykobaktériami sa vyskytuje z prostredia vzdušným prenosom, kontaktom s poškodením kože, ako aj prostredníctvom potravy a vody. Prenos mikroorganizmov z človeka na človeka je menej častý. Ide o oportúnne baktérie, takže pri rozvoji ochorenia má veľký význam zníženie rezistencie makroorganizmu a jeho genetická predispozícia. V postihnutých oblastiach sa tvoria granulómy. V závažných prípadoch je fagocytóza neúplná, bakterémia je výrazná a v orgánoch sa zisťujú makrofágy naplnené netuberkulóznymi mykobaktériami a bunkami pripomínajúcimi lepru.
Príznaky mykobakteriózy
Príznaky mykobakteriózy sú rôzne. Najčastejšie je postihnutý dýchací systém. Príznaky pľúcnej patológie sú podobné príznakom tuberkulózy. Často sa však vyskytujú prípady extrapulmonálnej lokalizácie procesu postihujúceho kožu a podkožné tkanivo, povrchy rán, lymfatické uzliny, urogenitálne orgány, kosti a kĺby, ako aj mozgové blany. Orgánové lézie môžu začať akútne aj latentne, ale takmer vždy prebiehajú závažne.
Možný je aj vývoj zmiešanej infekcie, v niektorých prípadoch môžu byť príčinou vzniku sekundárnej endogénnej infekcie.
Mikrobiologická diagnostika mykobakteriózy
Hlavnou metódou diagnostiky mykobakteriózy je bakteriologická. Materiál na štúdium sa odoberá na základe patogenézy a klinických prejavov ochorenia. Najprv sa rieši otázka, či izolovaná čistá kultúra patrí k pôvodcom tuberkulózy alebo k netuberkulóznym mykobaktériám. Potom sa použije súbor štúdií na stanovenie typu mykobaktérií, stupňa virulencie a Runyonovej skupiny. Primárna identifikácia je založená na znakoch, ako je rýchlosť rastu, schopnosť tvoriť pigment, morfológia kolónií a schopnosť rásť pri rôznych teplotách. Na identifikáciu týchto znakov nie je potrebné žiadne ďalšie vybavenie ani činidlá, takže sa môžu používať v základných laboratóriách tuberkulóznych dispenzárov. Konečná identifikácia (referenčná identifikácia) pomocou komplexných biochemických štúdií sa vykonáva v špecializovaných moratóriách vedeckých inštitúcií. Vo väčšine prípadov sa uprednostňuje ich identifikácia na základe biochemických faktov, pretože moderné molekulárne genetické metódy sú prácne, majú veľa prípravných fáz, vyžadujú si špeciálne vybavenie a sú drahé. Stanovenie citlivosti na antibiotiká má pre liečbu veľký význam. Kritérium súčasného výskytu klinických, rádiologických a laboratórnych údajov a izolácie čistej kultúry netuberkulóznych mykobaktérií, ako aj vykonanie viacerých dynamických štúdií, majú rozhodujúci význam pre diagnostiku mykobakteriózy.
V diagnostike má pomocný význam stanovenie antitéz pomocou RNGA, RP, imunoelektroforézy, RNIF a ELISA, ako aj vykonanie kožných alergických testov so senzitínmi.
Liečba a špecifická prevencia mykobakteriózy
Všetky typy netuberkulóznych mykobaktérií, s výnimkou M. xenopi, sú rezistentné na izoniazid, streptomycín a tiosemikarbazóny. Liečba mykobakteriózy antituberkulóznymi a antibakteriálnymi liekmi by mala byť dlhodobá (12 – 13 mesiacov) a kombinovaná. Zvyčajne je neúčinná pri infekciách MAC a ochoreniach spôsobených rýchlo rastúcimi mykobaktériami. V niektorých prípadoch sa používa chirurgická liečba. Lieky na špecifickú prevenciu mykobakteriózy neboli vyvinuté.


 [
[