Lekársky expert článku
Nové publikácie
Obvyklý potrat - príčiny
Posledná kontrola: 04.07.2025

Všetok obsah iLive je lekársky kontrolovaný alebo kontrolovaný, aby sa zabezpečila čo najväčšia presnosť faktov.
Máme prísne smernice týkajúce sa získavania zdrojov a len odkaz na seriózne mediálne stránky, akademické výskumné inštitúcie a vždy, keď je to možné, na lekársky partnerské štúdie. Všimnite si, že čísla v zátvorkách ([1], [2] atď.) Sú odkazmi na kliknutia na tieto štúdie.
Ak máte pocit, že niektorý z našich obsahov je nepresný, neaktuálny alebo inak sporný, vyberte ho a stlačte kláves Ctrl + Enter.
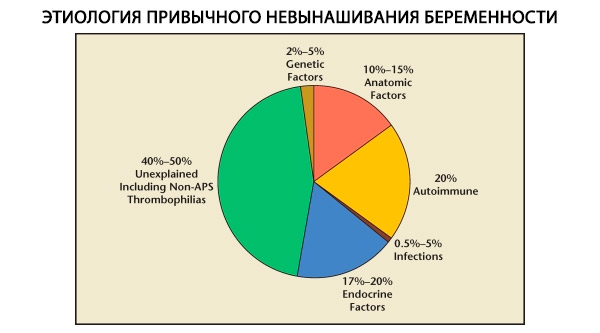
V štruktúre habituálnych potratov sa rozlišujú genetické, anatomické, endokrinné, imunologické a infekčné faktory. Po vylúčení všetkých vyššie uvedených príčin zostáva skupina pacientok, u ktorých je pôvod habituálneho potratu nejasný (idiopatické potraty). Podľa C. Coulama a kol. (1996) je 80 % idiopatických potratov spôsobených nerozpoznanými poruchami imunity.
Neexistujú presvedčivé dôkazy o tom, že endometrióza spôsobuje opakované potraty, alebo že medikamentózna alebo chirurgická liečba endometriózy znižuje výskyt opakovaných potratov.
Podľa súčasných koncepcií, okrem genetických a čiastočne infekčných príčin vedúcich k tvorbe abnormálneho embrya, realizácia škodlivého účinku iných faktorov (anatomických, endokrinných, imunologických) spočíva vo vytvorení nepriaznivého pozadia pre vývoj geneticky kompletného oplodneného vajíčka, čo vedie k vyčerpaniu rezervnej kapacity choriónu a zastaveniu vývoja (embryogenéza). Kritické obdobia v prvom trimestri tehotenstva sa považujú za 6-8 týždňov (smrť embrya) a 10-12 týždňov (vylúčenie oplodneného vajíčka).
 [ 1 ]
[ 1 ]
Genetické príčiny habituálneho potratu
Genetické faktory predstavujú 3–6 % príčin habituálnych potratov. Pri sporadických prerušeniach tehotenstva v prvom trimestri má približne 50 % potratov chromozómové abnormality. Väčšina z nich (95 %) sú zmeny v počte chromozómov – monozómia (strata jedného chromozómu), trizómia (prítomnosť ďalšieho chromozómu), ktoré sú výsledkom chýb v meióze, ako aj polyploidia (zvýšenie zloženia chromozómov o celú haploidnú sadu), ktorá vzniká pri oplodnení vajíčka dvoma alebo viacerými spermiami. Pri sporadických potratoch sa najčastejšie vyskytuje trizómia – 60 % všetkých mutácií (najčastejšie na chromozóme 16, ako aj 13, 18, 21, 22), na druhom mieste vo frekvencii je Šereševskij-Turnerov syndróm (chromozóm 45 X0) – 20 %, zvyšných 15 % pripadá na polyploidiu (najmä triploidiu).
V prípade zmeny počtu chromozómov pri potrate vyšetrenie karyotypu rodičov najčastejšie neodhalí žiadnu patológiu a pravdepodobnosť chromozómového ochorenia plodu počas následného tehotenstva je 1 %. Naopak, pri vyšetrení potratov u párov s habituálnym potratom sa štrukturálne zmeny chromozómov (intra- a interchromozomálne) pozorujú v 3 – 6 % prípadov. Pri vyšetrení karyotypu rodičov sa vyvážené chromozómové prestavby nachádzajú v 7 % prípadov. Najčastejšie ide o recipročné translokácie, pri ktorých sa segment jedného chromozómu nachádza na mieste iného segmentu nehomologického chromozómu, ako aj o mozaiku pohlavných chromozómov, inverziu a detekciu chromozómov vo forme kruhu. V prípade prítomnosti takýchto prestavieb u jedného z manželov sú procesy párovania a separácie chromozómov počas meiózy narušené, čo má za následok stratu (deléciu) alebo zdvojenie (duplikáciu) chromozómových úsekov v gamétach. Výsledkom sú tzv. nevyvážené chromozomálne prestavby, pri ktorých je embryo buď neživotaschopné, alebo slúži ako nositeľ závažnej chromozomálnej patológie. Pravdepodobnosť narodenia dieťaťa s nevyváženými chromozomálnymi abnormalitami v prítomnosti vyvážených chromozomálnych prestavieb v karyotype jedného z rodičov je 1 – 15 %. Rozdiely v údajoch súvisia s povahou prestavieb, veľkosťou zúčastnených segmentov, pohlavím nositeľa a rodinnou anamnézou.
Diagnostika
Anamnéza
- Dedičné choroby u členov rodiny.
- Prítomnosť vrodených anomálií v rodine.
- Narodenie detí s mentálnou retardáciou.
- Prítomnosť neplodnosti a/alebo potratu neznámeho pôvodu u manželského páru alebo u príbuzných.
- Prítomnosť nejasných prípadov perinatálnej úmrtnosti.
Špeciálne výskumné metódy
- Štúdium karyotypu rodičov je obzvlášť indikované u manželských párov pri narodení novorodenca s vývojovými chybami okrem anamnézy potratu, ako aj v prípadoch habituálneho potratu v skorých štádiách tehotenstva.
- Cytogenetická analýza potratov v prípadoch mŕtvo narodeného dieťaťa alebo novorodeneckej úmrtnosti.
Indikácie pre konzultáciu s inými špecialistami
Ak sa u rodičov zistia zmeny v karyotype, je potrebná konzultácia s genetikom, aby sa posúdil stupeň rizika narodenia dieťaťa s patológiou alebo v prípade potreby sa rozhodlo o otázke darovania vajíčka alebo spermií.
Ďalšia liečba pacienta
Ak má manželský pár patologický karyotyp, a to aj u jedného z rodičov, odporúča sa vykonať prenatálnu diagnostiku počas tehotenstva - choriovú biopsiu alebo amniocentézu - kvôli vysokému riziku vývojových porúch u plodu.
Anatomické príčiny habituálneho potratu
Medzi anatomické príčiny habituálneho potratu patria:
- vrodené anomálie vo vývoji maternice (úplné zdvojenie maternice; dvojrohá, sedlovitá, jednorohá maternica; čiastočná alebo úplná vnútromaternicová priehradka);
- získané anatomické chyby;
- vnútromaternicové zrasty (Ashermanov syndróm);
- submukózne maternicové myómy;
- isthmicko-cervikálna insuficiencia.
Frekvencia anatomických anomálií u pacientok s habituálnym potratom sa pohybuje od 10 do 16 %. Frekvencia výskytu malformácií maternice, ktoré môžu viesť k potratu (ale nie k neplodnosti), vo vzťahu ku všetkým malformáciám maternice je nasledovná: dvojrohá maternica - 37 %, sedlovitá maternica - 15 %, vnútromaternicová priehradka - 22 %, úplné zdvojenie maternice - 11 %, jednorohá maternica - 4,4 %.
Diagnóza habituálneho potratu
Anamnéza
V prípade anatomickej patológie maternice sa častejšie pozorujú neskoré ukončenia tehotenstva a predčasné pôrody, avšak pri implantácii na vnútromaternicovej priehradke alebo v blízkosti myomatózneho uzla sú možné aj predčasné ukončenia tehotenstva.
Pri isthmicko-cervikálnej insuficiencii je patognomickým znakom spontánne ukončenie tehotenstva v druhom trimestri alebo skorý predčasný pôrod, ku ktorému dochádza pomerne rýchlo a s malou bolesťou.
V prípade malformácií maternice je potrebné venovať pozornosť anamnestickým indikáciám patológie močových ciest (často sprevádzajúcich vrodené anomálie maternice) a charakteru vývoja menštruačnej funkcie (indikácie hematometre s funkčným rudimentárnym rohom maternice).
Špeciálne vyšetrovacie metódy
- V súčasnosti sa na stanovenie diagnózy vykonáva hysterosalpingografia, ktorá umožňuje študovať tvar dutiny maternice, identifikovať prítomnosť submukóznych myómov, zrastov, sept a určiť priechodnosť vajíčkovodov. Na diagnostiku patológie maternice je racionálne vykonať hysterosalpingografiu v období medzi menštruáciou a ovuláciou, teda v prvej fáze menštruačného cyklu po ukončení krvácania (7. – 9. deň cyklu). Na diagnostiku isthmicko-cervikálnej insuficiencie sa vyšetrenie vykonáva v druhej fáze menštruačného cyklu (18. – 20. deň), aby sa zistil stav vnútorného ústia krčka maternice. Pred vykonaním hysterosalpingografie je potrebné vylúčiť zápalové ochorenia panvových orgánov alebo ich liečiť.
- Hysteroskopia sa v posledných rokoch rozšírila a stala sa zlatým štandardom v diagnostike vnútromaternicovej patológie. Vzhľadom na jej vyššie náklady v porovnaní s hysterosalpingografiou sa však táto metóda používa u žien s indikáciou vnútromaternicovej patológie na základe predbežných ultrazvukových údajov. Hysteroskopiou možno vyšetriť dutinu maternice, určiť povahu vnútromaternicovej patológie a ak je k dispozícii potrebné vybavenie (resektoskop), vykonať minimálne invazívnu chirurgickú liečbu - odstránenie zrastov, submukóznych myómových uzlín a endometriálnych polypov. Pri odstraňovaní vnútromaternicovej priehradky sa uprednostňuje hysteroresektoskopia s laparoskopickou kontrolou, ktorá zabraňuje možnosti perforácie steny maternice.
- Ultrazvuk sa vykonáva v prvej fáze menštruačného cyklu, čo umožňuje predpokladanú diagnózu submukózneho myómu maternice, vnútromaternicových zrastí a v druhej fáze cyklu - identifikovať vnútromaternicovú priehradku a dvojrohú maternicu. Táto metóda má osobitný význam v skorých štádiách tehotenstva, keď je jej citlivosť pri diagnostikovaní týchto stavov 100 % a jej špecificita je 80 %. Mimo tehotenstva si diagnóza vyžaduje dodatočné potvrdenie inými metódami.
- Zahraniční autori poukazujú na výhodu sonohysterografie (ultrazvuk s použitím transvaginálneho senzora s predchádzajúcim zavedením 0,9% roztoku chloridu sodného do dutiny maternice) oproti hysterosalpingografii, pretože umožňuje diferenciálnu diagnostiku medzi vnútromaternicovou priehradkou a dvojrohou maternicou. Pomocou sonohysterografie je možné nielen študovať tvar dutiny maternice, ale aj určiť konfiguráciu fundusu tela maternice. V našej krajine sa táto metóda nerozšírila.
- V niektorých zložitých prípadoch sa na overenie diagnózy používa magnetická rezonancia panvových orgánov. Metóda umožňuje získať cenné informácie v prípade vývojových anomálií maternice sprevádzaných atypickým usporiadaním orgánov v panve. MRI je dôležité v prípade rudimentárneho rohu maternice na rozhodnutie, či je vhodné ho odstrániť. Potreba odstrániť rudimentárny roh maternice nastáva v prípade jeho spojenia s vajíčkovodom a vaječníkom, aby sa zabránilo tvorbe a vývoju oplodneného vajíčka v ňom. Ukončenie tehotenstva v prípade anatomických anomálií maternice môže byť spojené s neúspešnou implantáciou oplodneného vajíčka (na vnútromaternicovej priehradke, v blízkosti submukózneho myómového uzla), nedostatočne vyvinutou vaskularizáciou a recepciou endometria, úzkymi priestorovými vzťahmi v dutine maternice (napríklad pri deformácii dutiny myómovým uzlom), často sprevádzanými ICI, a hormonálnymi poruchami.
Liečba habituálneho potratu
Chirurgická liečba
V prítomnosti vnútromaternicového septa, submukóznych myómových uzlín a zrastí je najúčinnejšou chirurgickou liečbou hysteroresektoskopia. Frekvencia následných potratov v tejto skupine žien po liečbe je 10 % v porovnaní s 90 % pred operáciou. Pri porovnaní výsledkov metroplastiky vykonanej laparotómiou a transcervikálnou hysteroresektoskopiou P. Heinonen (1997) dosiahol výsledky naznačujúce menšiu traumu a väčšiu účinnosť hysteroresektoskopie; percento tehotenstiev, ktoré viedli k narodeniu životaschopných detí, bolo 68 % a 86 %.
Chirurgické odstránenie vnútromaternicovej priehradky, zrastov a submukóznych myómových uzlín eliminuje potrat v 70 – 80 % prípadov. Je však neúčinné u žien s malformáciami maternice, ktoré mali normálny pôrod s následnými opakovanými potratmi. Je pravdepodobné, že v takýchto prípadoch nie je anatomický faktor hlavnou príčinou a je potrebné hľadať iné príčiny potratu.
Bolo dokázané, že abdominálna metroplastika je spojená s významným rizikom pooperačnej neplodnosti a nezlepšuje prognózu následného tehotenstva. Preto je lepšie uprednostniť hysteroskopiu a laparoskopické operácie.
Liečba drogovou závislosťou
Účinnosť zavedenia vnútromaternicového telieska, vysokých dávok estrogénových liekov, zavedenia Foleyho katétra do dutiny maternice po operáciách na odstránenie zrastov, vnútromaternicového septa nebola preukázaná. Odporúča sa plánovať tehotenstvo najskôr 3 mesiace po operácii. Na zlepšenie rastu endometria sa vykonáva cyklická hormonálna terapia počas 3 menštruačných cyklov [14]. Počas 3 mesiacov v prvých 14 dňoch cyklu sa odporúča užívať liek obsahujúci 2 mg 17-beta-estradiolu, v nasledujúcich 14 dňoch - 2 mg 17-beta-estradiolu a 20 mg dydrogesterónu (10 mg dydrogesterónu ako súčasť kombinovaného lieku plus 10 mg dydrogesterónu v samostatnej tabletovej forme).
Ďalšia liečba pacienta
Charakteristiky priebehu tehotenstva s dvojrohou maternicou alebo zdvojenou maternicou (ak sú prítomné 2 maternicové dutiny):
- v počiatočných štádiách tehotenstva sa krvácanie často vyskytuje z „prázdneho“ rohu alebo dutiny maternice v dôsledku výraznej deciduálnej reakcie; taktika v tomto prípade by mala byť konzervatívna a mala by pozostávať z použitia antispazmodických a hemostatických látok;
- hrozba ukončenia tehotenstva v rôznych štádiách;
- rozvoj isthmicko-cervikálnej insuficiencie;
- intrauterinná retardácia rastu v dôsledku placentárnej insuficiencie.
V počiatočných štádiách tehotenstva sa pri krvácaní odporúča pokoj na lôžku a čiastočný pokoj na lôžku, podávanie hemostatických, antispazmodických a sedatívnych liekov a liečba gestagénmi (dydrogesterón v dennej dávke 20 až 40 mg) až do 16–18. týždňa tehotenstva.
Endokrinné príčiny habituálneho potratu
Podľa rôznych autorov endokrinné príčiny potratu predstavujú 8 až 20 %. Najvýznamnejšie z nich sú deficit luteálnej fázy (LPD), hypersekrécia LH, dysfunkcia štítnej žľazy a diabetes mellitus.
Závažné ochorenie štítnej žľazy alebo diabetes mellitus môžu viesť k opakovaným potratom. Pri kompenzovanom diabete mellitus sa však riziko habituálnych potratov nelíši od rizika v bežnej populácii.
Zároveň vysoký výskyt hypotyreózy v populácii si vyžaduje skríning s meraním hladín TSH. U pacientok s habituálnym potratom sa insuficiencia luteálnej fázy pozoruje v 20 – 60 % prípadov a ultrazvukové príznaky polycystických vaječníkov v 44 – 56 %. Podľa literatúry zostáva vplyv jednotlivých hormonálnych porúch na tvorbu komplexu symptómov habituálneho potratu kontroverzný. Štúdie M. Ogasawaru a kol. (1997) neodhalili spoľahlivé rozdiely vo frekvencii ukončenia tehotenstva s LPI a bez nej u pacientok s dvoma alebo viacerými predchádzajúcimi potratmi v anamnéze, s vylúčením autoimunitných, anatomických a infekčných príčin.
Nedostatočná funkcia žltého telieska môže byť výsledkom viacerých nepriaznivých faktorov:
- poruchy sekrécie FSH a LH v prvej fáze menštruačného cyklu;
- skorý alebo naopak príliš neskorý vrchol uvoľňovania LH;
- hypoestrogénia ako dôsledok nedostatočnej folikulogenézy. Všetky tieto stavy nie sú korigovateľné substitučnou terapiou gestagénovými liekmi v postovulačnom období. Prospektívne štúdie, ktoré vykonali L. Regan a kol., preukázali významný nárast frekvencie potratov u pacientok s hypersekréciou LH na 8. deň menštruačného cyklu v porovnaní so ženami s normálnymi hladinami LH v krvi (65 % a 12 % potratov). Škodlivý účinok predčasného nárastu LH je spojený s predčasným obnovením druhého meiotického delenia a ovulácie nezrelého vajíčka, ako aj s indukciou produkcie androgénov bunkami theka spolu so zhoršenou endometriálnou recepciou pod vplyvom gestagénovej insuficiencie. Predbežné zníženie preovulačných hladín LH agonistami hormónu uvoľňujúceho gonadotropín bez ďalších opatrení zameraných na predĺženie následného tehotenstva však neposkytuje očakávané zníženie frekvencie potratov.
Zlatým štandardom pre diagnostiku NLF je histologické vyšetrenie materiálu získaného z biopsie endometria v druhej fáze cyklu počas 2 menštruačných cyklov.
Diagnózu iných príčin ovulačnej dysfunkcie, ako je hyperprolaktinémia, hypotyreóza, funkčný nadbytok androgénov (vaječníkov alebo nadobličiek), musí sprevádzať predpísanie vhodnej liečby.
Diagnostika
Anamnéza a fyzikálne vyšetrenie
- Anamnéza. Faktory, ktoré treba zvážiť: neskorá menarcha, nepravidelný menštruačný cyklus (oligomenorea, amenorea, náhle priberanie na váhe, úbytok hmotnosti, neplodnosť, habituálne skoré potraty).
- Vyšetrenie: typ postavy, výška, telesná hmotnosť, hirsutizmus, závažnosť sekundárnych pohlavných znakov, prítomnosť strií, vyšetrenie mliečnych žliaz na galaktoreu.
- Funkčné diagnostické testy: meranie rektálnej teploty počas 3 menštruačných cyklov.
Špeciálne výskumné metódy
- Hormonálna štúdia:
- v 1. fáze menštruačného cyklu (7. – 8. deň) – stanovenie obsahu FSH, LH, prolaktínu, TSH, testosterónu, 17-hydroxyprogesterónu (17-OP), DHEAS;
- v 2. fáze menštruačného cyklu (21–22 dní) – stanovenie obsahu progesterónu (normatívne ukazovatele hladín progesterónu sú veľmi variabilné, metódu nemožno použiť bez zohľadnenia ďalších faktorov).
- Ultrazvuk:
- v 1. fáze menštruačného cyklu (5. – 7. deň) – diagnostika patológie endometria, polycystických vaječníkov;
- v 2. fáze menštruačného cyklu (20–21 dní) – meranie hrúbky endometria (normálna 10–11 mm, koreluje s obsahom progesterónu).
- Biopsia endometria na overenie NLF sa vykonáva 2 dni pred očakávanou menštruáciou (26. deň pri 28-dňovom cykle). Táto metóda sa používa v prípadoch, keď je diagnóza nejasná. Na štúdium zmien v endometriu v tzv. období „implantačného okna“ sa biopsia vykonáva 6. deň po ovulácii.
Liečba
Pri diagnostikovaní NLF (podľa rektálnych teplotných grafov je trvanie 2. fázy kratšie ako 11 dní, pozoruje sa postupné zvyšovanie teploty, nedostatočná sekrečná transformácia endometria podľa údajov z biopsie endometria, nízke hladiny progesterónu v krvnom sére) je potrebné identifikovať príčinu takýchto porúch.
Ak je NLF sprevádzaná hyperprolaktinémiou, vykoná sa MRI mozgu. Alternatívnou metódou je röntgen lebky (oblasť tureckého sedla).
Prvým štádiom hyperprolaktinémie je vylúčenie adenómu hypofýzy, ktoré si vyžaduje chirurgickú liečbu. Pri absencii významných zmien sa hyperprolaktinémia považuje za funkčnú a na normalizáciu hladín prolaktínu sa predpisuje liečba bromokriptínom. Počiatočná dávka bromokriptínu je 1,25 mg/deň počas 2 týždňov, po monitorovaní hladín prolaktínu, ak sa ukazovatele nenormalizujú, sa dávka zvýši na 2,5 mg/deň. Pri významnom zvýšení hladín prolaktínu je počiatočná dávka 2,5 mg/deň. Ak dôjde k otehotneniu, bromokriptín sa má vysadiť.
Ak sa zistí hypotyreóza, charakter patológie štítnej žľazy sa určí spolu s endokrinológom. V každom prípade je indikovaná denná liečba levotyroxínom sodným, dávka sa volí individuálne, kým sa hladina TSH normalizuje. Ak dôjde k otehotneniu, liečba levotyroxínom sodným by mala pokračovať. Otázka vhodnosti zvýšenia dávky v prvom trimestri tehotenstva sa rozhoduje spolu s endokrinológom po obdržaní výsledkov hormonálneho vyšetrenia (hladina TSH, voľný tyroxín).
Korekcia NLF sa vykonáva jedným z dvoch spôsobov. Prvým spôsobom je stimulácia ovulácie, druhým spôsobom je substitučná terapia progesterónovými prípravkami.
Prvou možnosťou liečby je stimulácia ovulácie klomiféncitrátom. Táto liečebná metóda je založená na skutočnosti, že väčšina porúch luteálnej fázy sa prejavuje vo folikulárnej fáze cyklu. Konštantne znížené hladiny progesterónu v 2. fáze sú dôsledkom zhoršenej folikulogenézy v 1. fáze cyklu. Táto porucha sa dá s väčším úspechom korigovať nízkymi dávkami klomiféncitrátu v skorej folikulárnej fáze ako predpisovaním progesterónu v 2. fáze cyklu.
V 1. cykle je dávka klomiféncitrátu 50 mg/deň od 5. do 9. dňa menštruačného cyklu. Účinnosť sa monitoruje pomocou rektálnych teplotných grafov, meraní hladiny progesterónu v 2. fáze cyklu alebo dynamického ultrazvuku. Ak nie je dostatočný účinok v 2. cykle stimulácie ovulácie, dávka klomiféncitrátu sa má zvýšiť na 100 mg/deň od 5. do 9. dňa cyklu. Maximálna možná dávka v 3. cykle stimulácie ovulácie je 150 mg/deň. Takéto zvýšenie dávky je možné len vtedy, ak je liek dobre tolerovaný (žiadna intenzívna bolesť v podbrušku a krížoch a žiadne iné príznaky ovariálnej hyperstimulácie).
Druhá možnosť liečby: substitučná terapia progesterónovými prípravkami, ktoré podporujú úplnú sekrečnú transformáciu endometria, čo poskytuje potrebný účinok u pacientok s habituálnym potratom so zachovanou ovuláciou. Okrem toho sa v posledných rokoch zistilo, že podávanie progesterónových prípravkov má nielen hormonálny, ale aj imunomodulačný účinok, potláča rejekčné reakcie imunokompetentných buniek v endometriu. Podobný účinok bol opísaný najmä pri dihydrogesteróne v dávke 20 mg/deň. Na účely substitučnej terapie sa dydrogesterón používa perorálne v dávke 20 mg/deň alebo mikronizovaný progesterón vaginálne v dávke 200 mg/deň. Liečba sa vykonáva druhý deň po ovulácii (deň po zvýšení rektálnej teploty) a pokračuje 10 dní. Ak dôjde k otehotneniu, liečba progesterónovými prípravkami by mala pokračovať.
Moderný výskum nepotvrdil účinnosť ľudského choriového gonadotropínu pri liečbe opakovaných potratov.
Pri hyperandrogenizme (ovariálny alebo adrenálny pôvod) u pacientok s habituálnym potratom je indikovaná liečba liekmi kvôli vplyvu androgénov na úplnosť ovulácie a stav endometria. V prípade porušenia biosyntézy adrenálnych androgénov je možný ich virilizačný účinok na ženský plod, preto sa steroidná terapia vykonáva v záujme plodu.
Hyperandrogénnosť ovariálneho pôvodu (polycystické vaječníky)
Anamnéza, fyzikálne vyšetrenie a výsledky špeciálneho vyšetrenia
- Anamnéza: neskorá menarcha, poruchy menštruačného cyklu ako oligomenorea (zvyčajne primárna, menej často sekundárna). Tehotenstvá sú zriedkavé, zvyčajne spontánne prerušené v prvom trimestri, s dlhými obdobiami neplodnosti medzi tehotenstvami.
- Vyšetrenie: hirsutizmus, akné, strie, vysoký index telesnej hmotnosti (voliteľné).
- Rektálne teplotné grafy: anovulačné cykly sa striedajú s cyklami s ovuláciou a NLF.
- Hormonálne vyšetrenie: vysoké hladiny testosterónu, môžu byť zvýšené hladiny FSH a LH, pomer LH/FSH je väčší ako 3. Ultrazvuk: polycystické vaječníky.
Liečba
Nelieková liečba
Chudnutie - diétna terapia, fyzická aktivita.
Liečba drogovou závislosťou
- Orlistat v dávke 120 mg s každým hlavným jedlom. Trvanie liečby sa určuje s ohľadom na účinok a znášanlivosť.
- Predbežné zníženie testosterónu prípravkami obsahujúcimi cyproterónacetát (2 mg) a EE (35 mcg) počas 3 menštruačných cyklov.
- Vysadenie antikoncepcie, hormonálna podpora druhej fázy cyklu (gestagénová terapia) - dydrogesterón v dávke 20 mg/deň od 16. do 25. dňa menštruačného cyklu. Ak nedôjde k spontánnej ovulácii, prejsť do ďalšej fázy.
- Stimulácia ovulácie klomiféncitrátom v počiatočnej dávke 50 mg/deň od 5. do 9. dňa menštruačného cyklu so súčasnou liečbou gestagénmi (dydrogesterón v dávke 20 mg/deň od 16. do 25. dňa cyklu) a dexametazónom (0,5 mg).
- V prípade absencie tehotenstva sa dávka klomiféncitrátu zvyšuje na 100 – 150 mg/deň podávaním gestagénov v druhej fáze cyklu a dexametazónu (0,5 mg). Bolo zistené, že hoci dexametazón znižuje iba hladinu nadobličkových androgénov, ovulácia a počatie sa vyskytujú pri liečbe klomiféncitrátom a dexametazónom výrazne častejšie ako pri použití samotného klomiféncitrátu [12].
- Vykonávajú sa tri cykly stimulácie ovulácie, po ktorých sa odporúča prerušenie troch menštruačných cyklov s gestagénnou podporou a rozhodnutie o chirurgickej liečbe s využitím laparoskopického prístupu (klinová resekcia vaječníkov, laserová vaporizácia).
Ďalšia liečba pacienta
Manažment tehotenstva by mal byť sprevádzaný gestagénnou podporou až do 16. týždňa tehotenstva (dydrogesterón v dávke 20 mg/deň alebo mikronizovaný progesterón v dávke 200 mg/deň), dexametazón sa predpisuje iba v prvom trimestri tehotenstva. Monitorovanie je povinné pre včasnú diagnostiku isthmicko-cervikálnej insuficiencie a v prípade potreby jej chirurgickú korekciu.
Adrenálny hyperandrogénizmus (pubertálny a postpubertálny adrenogenitálny syndróm)
Adrenogenitálny syndróm (AGS) je dedičné ochorenie spojené s poruchou syntézy hormónov kôry nadobličiek v dôsledku poškodenia génov zodpovedných za syntézu viacerých enzýmových systémov. Ochorenie sa dedí autozomálne recesívne s prenosom mutantných génov od oboch rodičov, ktorí sú zdravými nosičmi.
V 90 % prípadov je adrenogenitálny syndróm spôsobený mutáciami v géne CYP21B, čo vedie k narušeniu syntézy 21-hydroxylázy.
Anamnéza, fyzikálne vyšetrenie a výsledky špeciálneho vyšetrenia
- Anamnéza: neskorá menarcha, mierne predĺžený menštruačný cyklus, možná oligomenorea, spontánne potraty v prvom trimestri, možná neplodnosť.
- Vyšetrenie: akné, hirsutizmus, androidný typ postavy (široké ramená, úzka panva), hypertrofia klitorisu.
- Rektálne teplotné grafy: anovulačné cykly sa striedajú s cyklami s ovuláciou a NLF.
- Hormonálny test: vysoké hladiny 17-OP, DHEAS.
- Ultrazvuk: vaječníky sú nezmenené.
Patognomickým znakom mimo tehotenstva je zvýšenie koncentrácie 17-OP v krvnej plazme.
V súčasnosti sa na diagnostiku latentnej, neklasickej formy adrenálneho hyperandrogénizmu používa test s ACTH. Na tento test sa používa Synacthen - syntetický polypeptid, ktorý má vlastnosti endogénneho ACTH, teda stimuluje počiatočné fázy syntézy steroidných hormónov z cholesterolu v nadobličkách.
Synacthenový test (analóg ACTH): 1 ml (0,5 mg) synacthenu sa vstrekne subkutánne do ramena, počiatočný obsah 17-OP a kortizolu sa najprv stanoví v rannej 9-hodinovej vzorke krvnej plazmy. Kontrolná vzorka krvi sa odoberie 9 hodín po injekcii na stanovenie hladiny 17-OP a kortizolu. Index stanovenia (D) sa potom vypočíta pomocou vzorca:
D = 0,052 × 17-OP + 0,005 × kortizol/17-OP - 0,018 × kortizol/17-OP
Ak je koeficient D menší alebo rovný 0,069, naznačuje to absenciu adrenálneho hyperandrogénneho ochorenia. Ak je koeficient D väčší ako 0,069, malo by sa predpokladať, že hyperandrogénny syndróm je spôsobený dysfunkciou nadobličiek.
Liečba drogovou závislosťou
Hlavnou liečbou hyperandrogénneho syndrómu spôsobeného deficitom 21-hydroxylázy sú glukokortikoidy, ktoré sa používajú na potlačenie nadmernej sekrécie androgénov.
Ďalšia liečba pacienta
Vzhľadom na virilizačný účinok materských androgénov na plod sa pri stanovenej diagnóze adrenálneho hyperandrogénizmu liečba dexametazónom v počiatočnej dávke 0,25 mg predpisuje pred tehotenstvom a pokračuje v individuálne zvolenej dávke (od 0,5 do 1 mg) počas celého tehotenstva. U ženy s habituálnym potratom trpiacej adrenálnym hyperandrogénizmom nie je vhodné liečbu zrušiť, pretože frekvencia potratov bez liečby dosahuje 14 % a pri pokračovaní liečby 9 %.
Vzhľadom na to, že pacientky s adrenogenitálnym syndrómom môžu tento gén preniesť na plod, je potrebné vykonať prenatálnu diagnostiku: v 17. – 18. týždni tehotenstva sa predpíše krvný test na stanovenie obsahu 17-OP u matky. Ak je hladina hormónu v krvi zvýšená, určí sa jeho koncentrácia v plodovej vode. Ak je obsah 17-OP v plodovej vode zvýšený, diagnostikuje sa adrenogenitálny syndróm u plodu. Bohužiaľ, nie je možné určiť závažnosť adrenogenitálneho syndrómu (mierna alebo ťažká forma s úbytkom soli) podľa hladiny 17-OP v plodovej vode. Otázku zachovania tehotenstva v tejto situácii rozhodujú rodičia.
Ak je otec dieťaťa nositeľom génu adrenogenitálneho syndrómu a v rodine sa vyskytli prípady detí narodených s týmto syndrómom, potom pacientka, aj bez adrenálneho hyperandrogenizmu, dostáva v záujme plodu dexametazón (na prevenciu virilizácie ženského plodu) v dávke 20 mcg/kg telesnej hmotnosti, maximálne 1,5 mg/deň v 2-3 dávkach po jedle. V 17.-18. týždni, po určení pohlavia plodu a expresie génu adrenogenitálneho syndrómu (na základe výsledkov amniocentézy), sa v liečbe pokračuje až do konca tehotenstva, ak je plod dievča s adrenogenitálnym syndrómom. Ak je plod chlapec alebo dievča, ktoré nie je nositeľom génu adrenogenitálneho syndrómu, je možné dexametazón vysadiť.
Ak žena s habituálnym potratom trpí adrenálnym hyperandrogenizmom, liečba dexametazónom sa vykonáva počas celého tehotenstva a preruší sa až po pôrode. Na 3. deň po pôrode sa dávka dexametazónu postupne znižuje (o 0,125 mg každé 3 dni) až do úplného prerušenia liečby v popôrodnom období.
Hyperandrogénia zmiešaného pôvodu (vaječníkov a nadobličiek)
Anamnéza, fyzikálne vyšetrenie a výsledky špeciálneho vyšetrenia
- Anamnéza: neskorá menarcha, poruchy menštruačného cyklu ako oligomenorea (zvyčajne primárna, menej často sekundárna), amenorea, možné zranenia, otrasy mozgu. Tehotenstva sú zriedkavé, zvyčajne spontánne prerušené v prvom trimestri, dlhé obdobia neplodnosti medzi tehotenstvami.
- Fyzikálne vyšetrenie: hirsutizmus, akné, strie, acanthosis nigricans, vysoký index telesnej hmotnosti, hypertenzia.
- Rektálne teplotné grafy: anovulačné cykly sa striedajú s cyklami s ovuláciou a NLF.
- Hormonálne vyšetrenie: vysoké hladiny testosterónu, môžu byť zvýšené hladiny FSH a LH, pomer LH/FSH väčší ako 3, vysoké hladiny DHEAS, 17-OP, môže byť prítomná hyperprolaktinémia.
- Ultrazvuk: polycystické vaječníky.
- Elektroencefalografia: zmeny v bioelektrickej aktivite mozgu.
- Hyperinzulinémia, porucha metabolizmu lipidov (vysoký cholesterol, lipoproteíny s nízkou hustotou a lipoproteíny s veľmi nízkou hustotou), znížená glukózová tolerancia alebo zvýšené hladiny glukózy v krvi.
Liečba
Nelieková liečba
Chudnutie (nízkokalorická diéta, fyzická aktivita).
Liečba drogovou závislosťou
Prvá fáza - v prítomnosti inzulínovej rezistencie sa odporúča predpísať metformín v dennej dávke 1000-1500 mg na zvýšenie citlivosti na inzulín.
Druhá fáza - v prípade závažných porúch menštruačného cyklu a vysokých hladín testosterónu sa odporúča predpísať lieky s antiandrogénnym účinkom obsahujúce cyproterónacetát (2 mg) a etinylestradiol (35 mcg) počas 3 mesiacov.
Treťou fázou je stimulácia ovulácie, po ktorej nasleduje gestagénna podpora (schéma je opísaná vyššie) a užívanie dexametazónu v dennej dávke 0,25–0,5 mg.
V prípade hyperprolaktinémie a hypotyreózy je potrebné vykonať vhodnú úpravu liečby v cykloch stimulácie ovulácie. Ak dôjde k otehotneniu, bromokriptín sa má vysadiť a levotyroxín sa má podávať ďalej.
Ak je stimulácia ovulácie neúčinná, malo by sa rozhodnúť o otázke predpísania priamych induktorov ovulácie, vhodnosti chirurgickej liečby polycystických vaječníkov alebo oplodnenia in vitro.
Ďalšia liečba pacienta
U pacientok s metabolickým syndrómom je tehotenstvo často komplikované arteriálnou hypertenziou, nefropatiou, hyperkoaguláciou, v súvislosti s ktorými je potrebné monitorovať krvný tlak, hemostaziogramy od skorých štádií tehotenstva a korigovať vznikajúce poruchy (ak je to potrebné) antihypertenzívami, antiagregačnými látkami a antikoagulanciami. Gestagénne lieky sa predpisujú do 16 týždňov tehotenstva - didrogesterón v dávke 20 mg / deň alebo mikronizovaný progesterón v dávke 200 mg / deň v 2 dávkach.
Všetky ženy s hyperandrogénnym syndrómom predstavujú rizikovú skupinu pre rozvoj isthmicko-cervikálnej insuficiencie. Monitorovanie stavu krčka maternice by sa malo vykonávať od 16. týždňa tehotenstva, v prípade potreby - chirurgická korekcia isthmicko-cervikálnej insuficiencie.
Imunologické príčiny habituálneho potratu
V súčasnosti je známe, že približne 80 % všetkých predtým nevysvetlených prípadov opakovaných potratov (po vylúčení genetických, anatomických a hormonálnych príčin) súvisí s poruchami imunity. Rozlišujú sa autoimunitné a aloimunitné poruchy, ktoré vedú k habituálnemu potratu.
Pri autoimunitných procesoch sa objektom agresie stávajú vlastné tkanivá imunitného systému, teda imunitná odpoveď je namierená proti vlastným antigénom. V tejto situácii plod trpí sekundárne v dôsledku poškodenia tkanív matky.
Pri aloimunitných poruchách je imunitná odpoveď ženy namierená proti embryonálnym/fetálnym antigénom prijatým od otca, ktoré sú potenciálne cudzie pre telo matky.
Medzi autoimunitné poruchy, ktoré sa najčastejšie vyskytujú u pacientok s habituálnym potratom, patrí prítomnosť antifosfolipidových, antityreoidálnych a antinukleárnych autoprotilátok v sére. Zistilo sa teda, že 31 % žien s habituálnym potratom mimo tehotenstva má autoprotilátky proti tyreoglobulínu a tyreoidálnej peroxidáze (tyreoidálne mikrozomálne [tyreoidálna peroxidáza] autoprotilátky); v týchto prípadoch sa riziko spontánneho potratu v prvom trimestri tehotenstva zvyšuje na 20 %. Pri habituálnom potratoch prítomnosť antinukleárnych a antityreoidálnych protilátok naznačuje potrebu ďalšieho vyšetrenia na identifikáciu autoimunitného procesu a overenie diagnózy.
Antifosfolipidový syndróm (APS) zostáva všeobecne uznávaným autoimunitným ochorením vedúcim k úmrtiu embrya/plodu.
Aloimunitné poruchy
V súčasnosti aloimunitné procesy vedúce k odmietnutiu plodu zahŕňajú prítomnosť zvýšeného (viac ako 3) počtu spoločných antigénov hlavného systému histokompatibilného komplexu u manželov (často pozorovaného v pokrvných manželstvách); nízke hladiny blokujúcich faktorov v sére matky; zvýšené hladiny prirodzených zabíjačských buniek (NK bunky CD56, CD16) v endometriu a periférnej krvi matky mimo tehotenstva aj počas neho; vysoké hladiny koncentrácie mnohých cytokínov v endometriu a krvnom sére, najmä γ-interferónu, faktora nekrózy nádorov a, interleukínov-1 a 2.
V súčasnosti sa skúmajú aloimunitné faktory vedúce k skorým potratom tehotenstva a spôsoby nápravy vyššie uvedených stavov. Neexistuje konsenzus o metódach liečby. Podľa niektorých výskumníkov aktívna imunizácia darcovskými lymfocytmi neprináša významný účinok, zatiaľ čo iní autori opisujú významný pozitívny účinok pri takejto imunizácii a liečbe imunoglobulínmi.
V súčasnosti je jedným z imunomodulačných činidiel v ranom tehotenstve progesterón. Štúdie preukázali najmä úlohu dydrogesterónu v dennej dávke 20 mg u žien s habituálnym potratom v prvom trimestri tehotenstva so zvýšenou hladinou buniek CD56 v endometriu.
 [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ], [ 16 ]
[ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ], [ 16 ]
Geneticky podmienené trombofílie
Nasledujúce formy geneticky podmienených trombofílií sa považujú za trombofilné stavy počas tehotenstva vedúce k habituálnemu potratu.
- Nedostatok antitrombínu III.
- Mutácia faktora V (Leidenská mutácia).
- Nedostatok proteínu C.
- Nedostatok proteínu S.
- Mutácia génu protrombínu G20210A.
- Hyperhomocysteinémia.
Vyšetrenie na identifikáciu zriedkavých príčin trombofílie je potrebné v prípadoch, keď sa vyskytli:
- rodinná anamnéza - tromboembólia pred dosiahnutím veku 40 rokov u príbuzných;
- spoľahlivé epizódy venóznej a/alebo arteriálnej trombózy pred dosiahnutím veku 40 rokov;
- opakovaná trombóza u pacienta a jeho bezprostredných príbuzných;
- tromboembolické komplikácie počas tehotenstva a po pôrode pri užívaní hormonálnej antikoncepcie;
- opakované potraty, mŕtvo narodené deti, retardácia vnútromaternicového rastu, odlúčenie placenty;
- preeklampsia s včasným nástupom, HELLP syndróm.
Infekčné príčiny habituálneho potratu
Úloha infekčného faktora ako príčiny habituálneho potratu je v súčasnosti predmetom širokých diskusií. Je známe, že primárna infekcia v skorých štádiách tehotenstva môže spôsobiť poškodenie embrya, ktoré je nezlučiteľné so životom, čo vedie k sporadickým spontánnym potratom. Pravdepodobnosť reaktivácie infekcie súčasne s následkom opakovaných potratov je však zanedbateľná. Okrem toho sa v súčasnosti nenašli mikroorganizmy, ktoré by vyvolávali habituálny potrat. Štúdie z posledných rokov ukázali, že väčšina žien s habituálnym potratom a chronickou endometritídou má v endometriu prevalenciu 2 – 3 alebo viacerých typov obligátnych anaeróbnych mikroorganizmov a vírusov.
Podľa VM Sidelnikovej a kol. u žien trpiacich habituálnym potratom bola diagnóza chronickej endometritídy mimo tehotenstva histologicky overená v 73,1 % prípadov a v 86,7 % bola pozorovaná perzistencia oportúnnych mikroorganizmov v endometriu, čo môže byť určite príčinou aktivácie imunopatologických procesov. Zmiešaná perzistentná vírusová infekcia (vírus herpes simplex, Coxsackie A, Coxsackie B, enterovírusy 68–71, cytomegalovírus) sa u pacientok s habituálnym potratom vyskytuje výrazne častejšie ako u žien s normálnou pôrodníckou anamnézou. K. Kohut a kol. (1997) preukázali, že percento zápalových zmien v endometriu a deciduálnom tkanive u pacientok s primárnym opakovaným potratom je výrazne vyššie ako u žien po potrate s anamnézou aspoň jedného donoseného pôrodu.
Bakteriálna a vírusová kolonizácia endometria zvyčajne vyplýva z neschopnosti imunitného systému a nešpecifických ochranných síl tela (systém komplementu, fagocytóza) úplne eliminovať infekčný agens a zároveň je jeho šírenie obmedzené aktiváciou T-lymfocytov (T-helperov, prirodzených zabíjačov) a makrofágov. Vo všetkých vyššie uvedených prípadoch dochádza k perzistencii mikroorganizmov, ktorá sa vyznačuje priťahovaním mononukleárnych fagocytov, prirodzených zabíjačov, T-helperov, syntetizujúcich rôzne cytokíny, k miestu chronického zápalu. Zdá sa, že takýto stav endometria bráni vzniku lokálnej imunosupresie v preimplantačnom období, ktorá je nevyhnutná na vytvorenie ochrannej bariéry a zabránenie odmietnutia polocudzieho plodu.
V tejto súvislosti by sa u žien s habituálnym potratom mala pred otehotnením diagnostikovať chronická endometritída. Na stanovenie alebo vylúčenie tejto diagnózy sa vykonáva biopsia endometria na 7. – 8. deň menštruačného cyklu s histologickým vyšetrením, PCR a bakteriologickým vyšetrením materiálu z dutiny maternice. Pri overení diagnózy sa chronická endometritída lieči podľa štandardov pre liečbu zápalových ochorení panvových orgánov.

