Lekársky expert článku
Nové publikácie
Diagnostika štádií priebehu rakoviny prostaty
Last reviewed: 04.07.2025

Všetok obsah iLive je lekársky kontrolovaný alebo kontrolovaný, aby sa zabezpečila čo najväčšia presnosť faktov.
Máme prísne smernice týkajúce sa získavania zdrojov a len odkaz na seriózne mediálne stránky, akademické výskumné inštitúcie a vždy, keď je to možné, na lekársky partnerské štúdie. Všimnite si, že čísla v zátvorkách ([1], [2] atď.) Sú odkazmi na kliknutia na tieto štúdie.
Ak máte pocit, že niektorý z našich obsahov je nepresný, neaktuálny alebo inak sporný, vyberte ho a stlačte kláves Ctrl + Enter.
Klinicky sa rozlišuje medzi lokalizovaným (T1-2 , N0 , M0 ), lokálne pokročilým (T3-4 , N0-1 , M0 ) a generalizovaným karcinómom (T1-4 , N0-1 , M1 ).
Pacienti s klinicky lokalizovaným a lokálne pokročilým štádiom sú klasifikovaní podľa stupňa rizika (D'Amico A V. a kol., 2003):
- nízky: štádium T 1a-c; hladina PSA menej ako 10 ig/ml: Gleasonovo skóre - 2-5; v biopsii - jednostranná lézia menej ako 50 %:
- stredne ťažké: štádium T2a ; hladina PSA menej ako 10 ng/ml; Gleasonovo skóre - 3 + 4 = 7; v biopsii - bilaterálna lézia menej ako 50 %;
- vysoké štádium T2b , T3a -b; hladina PSA - 10-20 ng/ml; Gleasonovo skóre - viac ako 4 + 3 - 7; v biopsii - poškodenie viac ako 50 %, perineurálna invázia;
- veľmi vysoké: štádium T4 ; hladina PSA nad 20 ng/ml; Gleasonovo skóre nad 8; biopsia preukazuje lymfovaskulárnu inváziu.
Po objasnení diagnózy a stanovení rozsahu procesu (lokalizovaný, lokálne pokročilý alebo generalizovaný) stoja lekár a pacient pred výberom metódy liečby. V modernej spoločnosti sa prikladá veľký význam kvalite života pacientov po začatí liečby. Kvalita života bez liečby zodpovedá priebehu základného ochorenia a závisí od progresie onkologického procesu. Zmeny v kvalite života nastávajú najmä po začatí liečby a použití jednej z terapeutických alebo chirurgických metód. Jasné stanovenie štádia procesu umožňuje nielen zvoliť optimálnu metódu liečby, ale aj predpovedať ďalší priebeh ochorenia.
Stanovenie hladiny PSA v kombinácii s klinickým obrazom rakoviny prostaty a gradáciou nádoru podľa Gleasonovej stupnice významne zvyšuje informačný obsah každého z uvedených ukazovateľov pri stanovení patologického štádia rakoviny. AV Partin a kol. (1997) navrhli prognostické tabuľky, ktoré umožňujú predpovedať ďalšie šírenie nádoru, výber liečebnej metódy, stupeň radikality a prognózu účinnosti liečby.
Na posúdenie šírenia nádoru sa najčastejšie používajú metódy DRE, TRUS, stanovenie hladiny PSA a scintigrafia kostí. V prípade potreby sa predpisuje počítačová tomografia (CT) alebo magnetická rezonancia (MRI) a röntgen hrudníka.
Ktorákoľvek zo zobrazovacích metód je určená na určenie štádia a posúdenie účinnosti liečby. Po overení diagnózy musí urológ objasniť objem primárneho nádoru, jeho hranice, invazívny alebo metastatický potenciál nádoru. Všetky tieto ukazovatele majú veľký význam pre prognózu ochorenia a výber liečebnej metódy.
Primárny nádor (T)
V prvom rade je potrebné určiť, či je nádor obmedzený na prostatu (T 1-2 ) alebo presahuje kapsulu (T 3-4 ). Digitálne vyšetrenie často neumožňuje posúdiť rozšírenie nádoru. Podľa niektorých údajov výsledky DRE zodpovedajú výsledkom histologického vyšetrenia u menej ako 50 % pacientov. Podrobnejšie vyšetrenie je však indikované iba pri rozhodovaní o radikálnej liečbe.
Hladina PSA môže odrážať rozsah nádoru, ale neumožňuje presné určenie morfologického štádia. Kombinácia hladiny PSA, Gleasonovho indexu a palpačných údajov umožňuje lepšiu predpoveď morfologického štádia ako každý z týchto parametrov samostatne. Hodnota voľného PSA je kontroverzná: v jednej štúdii pomohlo stanovenie obsahu voľného PSA objasniť štádium lokalizovaných nádorov, ale iné štúdie to nepotvrdili. Túto otázku pomôžu vyriešiť iba hĺbkové štúdie.
Transrektálny ultrazvuk sa najčastejšie používa na vyšetrenie stavu prostaty. Táto metóda dokáže odhaliť iba 60 % nádorov a nie vždy ukazuje inváziu kapsuly. Takmer 60 % pacientov má štádium T3 . Ultrazvuk indikuje menej častý proces. Ultrazvukovými znakmi invázie kapsuly sú vydutie, nerovnosti a pretrhnutie kontúry žľazy. Invázia nádorových buniek do semenných vačkov je zlým prognostickým znakom, ale informácie o nej sú mimoriadne dôležité pre výber liečebnej metódy. Pri vykonávaní TRUS treba venovať pozornosť echostruktúre vezikúl (hyperechogenicita), ich asymetrii, deformácii a expanzii. Poškodenie semenných vačkov je tiež indikované stratou kruhovitosti a zhutnením na báze žľazy. Tieto znaky sú dosť subjektívne, preto nie je vhodné spoliehať sa výlučne na ultrazvukové údaje. Invázia semenných vačkov naznačuje vysoké riziko lokálneho relapsu a metastáz a na objasnenie (pred operáciou) je indikovaná ich biopsia. Vyšetrenie by sa nemalo začínať týmto postupom, ale ak je riziko invázie vysoké a výber liečby závisí od výsledku biopsie, potom je jeho vykonanie opodstatnené. Negatívny výsledok nevylučuje mikroskopickú inváziu. Biopsia semenných vačkov sa spravidla vykonáva v klinickom štádiu T 2b a vyššom a obsah PSA je vyšší ako 10 ng/ml. Výsledok sa považuje za pozitívny, ak aspoň jedna biopsia zo základne prostaty obsahuje nádorové bunky. Nielen ďalšie vyšetrenia, ale aj dôkladná analýza výsledkov primárnej biopsie umožňuje zvýšiť presnosť klinického určenia štádia (úlohu zohráva počet a rozsah nádorových ložísk, invázia kapsuly). Dôležitý je aj stupeň diferenciácie: pri Gleasonovom indexe menšom ako 6 je nádor lokalizovaný v 70 % prípadov.
Prietok krvi v prostate s rakovinou je vyšší ako v normálnej žľaze alebo s jej hyperpláziou. Po kastrácii je intenzita prietoku krvi v žľaze znížená. Vývoj echo-dopplerografických máp pre diagnostiku a monitorovanie rakoviny prostaty je sľubný, ale v súčasnosti neexistujú spoľahlivé údaje o použití echo-dopplerografie pri určovaní štádia lokálneho procesu. Túto metódu je možné použiť na získanie ďalšieho materiálu počas cielenej biopsie z ložísk patologickej vaskularizácie.
Výsledky vizualizácie rakoviny prostaty priamo závisia od technického vybavenia kliniky a skúseností špecialistu. Preto všetky moderné vizualizačné metódy nezohrávajú určujúcu, ale skôr objasňujúcu úlohu a výber liečebnej metódy je založený na kombinácii údajov z klinického vyšetrenia a inštrumentálnych štúdií.
Magnetická rezonancia (MRI) má najlepšie možnosti na vizualizáciu štruktúry prostaty. Moderným štandardom pre vyšetrenie panvových orgánov pomocou MRI metódy je použitie endorektálneho senzora, ktorý umožňuje získať obraz s najvyšším možným priestorovým rozlíšením 0,5-1 mm. Vháňanie vzduchu do endorektálneho senzora poskytuje jasnú vizualizáciu prostatickej kapsuly, rektoprostatických uhlov a Denonvilliersovej rektoprostatickej fascie. Použitie endorektálneho senzora pri MRI neobmedzuje vizualizáciu regionálnych lymfatických uzlín (až po úroveň bifurkácie brušnej aorty). Rakovina prostaty sa vyznačuje nízkou intenzitou signálu na T-vážených obrazoch na pozadí vysokointenzívneho signálu z nezmenenej periférnej zóny žľazy. Nepravidelný tvar, difúzne šírenie s hromadným efektom, rozmazané a nerovnomerné kontúry sú morfologickými charakteristikami ložísk s nízkou intenzitou signálu v periférnej zóne prostaty, čo naznačuje neoplastickú povahu lézie. Pri vykonávaní dynamickej kontrastnej látky rakovinové ložiská rýchlo akumulujú kontrastnú látku v arteriálnej fáze a rýchlo ju odstraňujú, čo odráža stupeň angiogenézy a podľa toho aj stupeň malignity nádoru. Nízka intenzita signálu je charakteristická aj pre ložiská krvácania po biopsii, prostatitídu, stromálnu benígnu hyperpláziu neutrálnej zóny žľazy, fibro-jazavé zmeny, fibromuskulárnu hyperpláziu, následky hormonálnej alebo rádioterapie. MRI bez dynamického kontrastu neumožňuje spoľahlivé rozlíšenie väčšiny uvedených zmien a ochorení.
Ako už bolo uvedené vyššie, jednou z hlavných úloh akejkoľvek zobrazovacej metódy pri rakovine prostaty je určenie objemu lézie žľazy a rozšírenia nádoru za jej puzdro. Stanovenie objemu nádoru je dôležité pre prognózu. Objem nádoru menší ako 4 cm3 naznačuje vzdialené metastázy a 12 cm3 naznačuje extrémne vysokú pravdepodobnosť metastáz. Podľa výskumu sa presnosť MRI pri detekcii ložísk neoplastických lézií prostaty pohybuje od 50 do 90 %. Citlivosť MRI pri určovaní lokalizácie rakoviny prostaty je približne 70 – 80 %, zatiaľ čo mikroskopické ložiská rakoviny (ložiská) nie je možné pomocou MRI zistiť.
Najdôležitejšou výhodou endorektálnej magnetickej rezonancie (MRI) je schopnosť lokalizovať neoplastické lézie v oblastiach neprístupných iným diagnostickým metódam a objasniť povahu a smer rastu nádoru. Napríklad MRI umožňuje detekciu neoplastických lézií v predných častiach periférnej zóny prostaty, ktoré nie sú dostupné transrektálnou biopsiou. Vo všeobecnosti MRI významne dopĺňa údaje DRE a TRUS o lokalizácii nádoru.
Endorektálna magnetická rezonancia umožňuje vizualizáciu puzdra žľazy, cievno-nervových zväzkov, semenných vačkov, vrcholu žľazy, periprostatického venózneho plexu a určenie lokálnej prevalencie nádoru žľazy. Treba zdôrazniť, že penetrácia puzdra sa považuje za mikroskopický znak a ani moderné MRI zariadenia (endorektálna cievka) nie sú schopné poskytnúť takéto informácie. Je možné získať iba údaje o raste za puzdro žľazy.
Diagnostické kritériá pre extrakapsulárne rozšírenie pomocou MRI:
- prítomnosť extrakapsulárneho nádoru;
- nerovný obrys žľazy (deformácia, uhlovitosť);
- asymetria neurovaskulárnych zväzkov;
- obliterácia rektoprostatických uhlov;
- široký kontakt nádoru s kapsulou.
Najvyššia špecificita (až 95-98 %) a presnosť výsledkov MRI sa dosahuje pri vyšetrení pacientov so stredným alebo vysokým rizikom extrakapsulárnej invázie. Predpokladá sa, že extrakapsulárna invázia (podľa údajov MRI) naznačuje nevhodnosť chirurgickej liečby a nepriaznivú prognózu ochorenia. Hormonálna alebo rádioterapia neovplyvňuje presnosť detekcie extrakapsulárneho šírenia nádoru prostaty. Hlavnou ťažkosťou pri detekcii ložísk rakoviny a extrakapsulárneho šírenia nádoru je vysoká variabilita interpretácie tomogramu rôznymi špecialistami. Primárnou úlohou špecialistu v radiačnej diagnostike je dosiahnuť vysokú diagnostickú špecificitu (aj na úkor citlivosti), aby operabilní pacienti neboli zbavení možnosti radikálnej liečby.
Podobnosť hustoty rakovinového, hyperplastického a normálneho tkaniva prostaty na CT robí túto metódu málo použiteľnou na posúdenie lokálneho šírenia nádoru. Invázia do semenných vačkov je dôležitejšia ako invázia do puzdier, ale aj v tomto prípade CT poskytuje informácie iba v pokročilých prípadoch. Táto metóda sa však aktívne používa na označenie oblasti zásahu pred rádioterapiou.
Pomalý rozvoj rádiodiagnostiky v našej krajine viedol k neskorej diagnostike rakoviny prostaty a následne k nedostatočnému rozšíreniu radikálnych metód liečby rakoviny prostaty (napríklad prostatektómia), nízkej dostupnosti moderných tomografov a absencii vhodných vzdelávacích programov pre špecialistov v rádiodiagnostike a urológov. Napriek tomu, že CT a MRI sú dnes rozšírené, úroveň vybavenia ordinácií a vzdelania špecialistov v rádiodiagnostike nie je dostatočná na to, aby získané informácie boli rozhodujúce pri výbere metódy liečby pacientov s rakovinou prostaty.
Regionálne lymfatické uzliny (N)
Regionálne lymfatické uzliny by sa mali hodnotiť iba vtedy, ak to priamo ovplyvňuje liečebnú stratégiu (zvyčajne pri plánovaní radikálnej liečby). Vysoké hladiny PSA, nádory T2c -T3a, slabá diferenciácia a perineurálna invázia sú spojené s vysokým rizikom metastáz do lymfatických uzlín. Hodnotenie stavu lymfatických uzlín na základe hladín PSA sa považuje za nedostatočné.
Iba lymfadenektómia (otvorená alebo laparoskopická) poskytuje potrebné informácie. Nedávne štúdie rozšírenej lymfadenektómie ukázali, že rakovina prostaty nie vždy postihuje obturátorové lymfatické uzliny. Pri asymptomatických nádoroch a hladinách PSA nižších ako 20 kg/ml CT potvrdí zväčšené lymfatické uzliny iba v 1 % prípadov. Použitie MRI alebo CT je opodstatnené v prípadoch vysokého rizika metastáz, pretože špecificita týchto metód dosahuje 93 – 96 %. Avšak aj pozitívny výsledok pri ich použití môže byť falošný a iba punkcia podozrivej lymfatické uzliny umožňuje odmietnuť lymfadenektómiu. Podľa retrospektívnej analýzy veľkosť lymfatických uzlín nie vždy naznačuje prítomnosť metastáz v nich; asymetria postihnutých lymfatických uzlín sa považuje za informatívnejší znak. V súčasnosti sú metastázy do lymfatických uzlín diagnostikované iba u 2 – 3 % pacientov, ktorí podstúpili radikálnu prostatektómiu pre lokalizovaný karcinóm prostaty, na základe pooperačného histologického vyšetrenia.
Ako metódy na detekciu metastáz do lymfatických uzlín sa odporúča pozitrónová emisná tomografia (PET) a scintigrafia so značenými protilátkami, ich použitie je však stále obmedzené kvôli nedostatočnej citlivosti.
Na posúdenie rizika postihnutia regionálnych lymfatických uzlín možno použiť Partinove nomogramy (2001). Nomogramy sú matematické algoritmy, ktoré sa používajú pre konkrétneho pacienta alebo skupinu pacientov. Tieto tabuľky umožňujú určiť pravdepodobnosť lokálneho šírenia nádoru (do kapsuly, semenných vačkov) a postihnutia lymfatických uzlín na základe klinického štádia, hladiny PSA a Gleasonovho indexu. Umožňujú najmä identifikovať skupinu pacientov s nízkou (menej ako 10 %) pravdepodobnosťou metastáz do lymfatických uzlín (s hladinou PSA nad 20 ng/md, štádiom T 1-2a a Gleasonovým indexom 2-6); v tejto skupine nemusí byť stav lymfatických uzlín pred radikálnou liečbou špecifikovaný. Riziko metastáz do lymfatických uzlín možno posúdiť aj detekciou oblastí nádoru s výraznou anapláziou (4-5 bodov): ak sa takéto oblasti nachádzajú v štyroch alebo viacerých biopsiách alebo prevládajú v aspoň jednej biopsii, riziko dosahuje 20-45 %. U ostatných pacientov nepresahuje 2,5 %. V takýchto prípadoch nie je potrebné dodatočné vyšetrenie.
Vzdialené metastázy (M)
U 85 % pacientov umierajúcich na rakovinu prostaty sa zisťujú lézie axiálneho skeletu. Kostné metastázy vznikajú v dôsledku prenikania rakovinových buniek do kostnej drene krvným obehom, čo vedie k rastu nádoru a lýze kostných štruktúr. Prevalencia kostných metastáz ovplyvňuje prognózu a ich včasné odhalenie varuje lekára pred možnými komplikáciami. V 70 % prípadov sú metastázy kombinované so zvýšením aktivity kostného izoenzýmu alkalickej fosfatázy (ALP). Stanovenie aktivity ALP a hladiny PSA nám v prevažnej väčšine prípadov umožňuje odhaliť kostné metastázy. Podľa multivariačnej analýzy sú tieto ukazovatele ovplyvnené iba počtom kostných metastáz. Je dôležité, aby aktivita kostného izoenzýmu ALP presnejšie odrážala stupeň poškodenia kostí ako hladina PSA.
Scintigrafia sa považuje za najcitlivejšiu metódu na detekciu kostných metastáz (je lepšia ako rádiografia a stanovenie aktivity alkalickej a kyslej fosfatázy). Technéciumdifosfonáty sa lepšie používajú ako rádiofarmakum, pretože ich akumulácia v kostiach je oveľa aktívnejšia ako v mäkkých tkanivách. Bola preukázaná korelácia medzi semikvantitatívnym hodnotením poškodenia kostí a prežitím. Detekcia vzdialených metastáz je možná v akomkoľvek orgáne. Najčastejšie sa vyskytujú v neregionálnych lymfatických uzlinách, pľúcach, pečeni, mozgu a koži. V prípade zodpovedajúcich ťažkostí a symptómov sa na ich detekciu používa röntgen hrudníka, ultrazvuk, CT a MRI. Taktika pri podozrení na kostné metastázy je uvedená na diagrame.
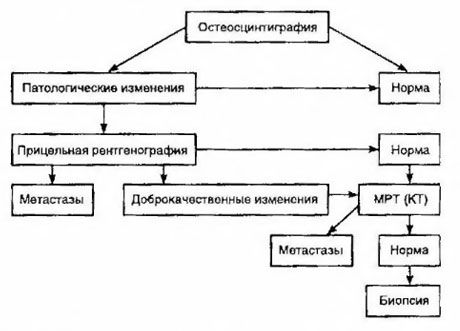
Najspoľahlivejším laboratórnym ukazovateľom, ktorý pomáha určiť stupeň metastáz, je hladina PSA. Ukázalo sa, že jej zvýšenie nad 100 ng/ml je jediný parameter, ktorý spoľahlivo indikuje vzdialené metastázy. Stanovenie hladiny PSA znižuje počet pacientov, ktorí potrebujú kostnú scintigrafiu. Pravdepodobnosť detekcie kostných metastáz pri zníženej hladine PSA je veľmi nízka. Pri absencii ťažkostí a počiatočnej hladine PSA nižšej ako 20 ng/ml, detekcii vysoko a stredne diferencovaných nádorov sa možno vyhnúť scintigrafii. Zároveň je v prípade slabo diferencovaných nádorov a invázie kapsuly indikovaná scintigrafia (bez ohľadu na hladinu PSA).


 [
[