Krvno-mozgová bariéra
Posledná kontrola: 23.04.2024

Všetok obsah iLive je lekársky kontrolovaný alebo kontrolovaný, aby sa zabezpečila čo najväčšia presnosť faktov.
Máme prísne smernice týkajúce sa získavania zdrojov a len odkaz na seriózne mediálne stránky, akademické výskumné inštitúcie a vždy, keď je to možné, na lekársky partnerské štúdie. Všimnite si, že čísla v zátvorkách ([1], [2] atď.) Sú odkazmi na kliknutia na tieto štúdie.
Ak máte pocit, že niektorý z našich obsahov je nepresný, neaktuálny alebo inak sporný, vyberte ho a stlačte kláves Ctrl + Enter.
Krvno-mozgová bariéra je mimoriadne dôležitá pre zabezpečenie homeostázy mozgu, ale mnohé otázky týkajúce sa jej formácie nie sú stále úplne pochopené. Ale už teraz je úplne jasné, že BBB je najvýraznejší na diferenciácii, zložitosti a hustote histohematologickej bariéry. Jeho hlavnou štruktúrnou a funkčnou jednotkou sú endotelové bunky kapilár mozgu.
Metabolizmus mozgu, podobne ako žiadny iný orgán, závisí od látok prichádzajúcich do krvného obehu. Množstvo krvných ciev poskytujúcich prácu nervového systému sa vyznačuje tým, že proces prenikania látok cez ich steny je selektívny. Endotelové bunky kapilár v mozgu sú spojené nepretržitými kontinuálnymi kontaktmi, takže látky môžu prechádzať iba cez samotné bunky, ale nie medzi nimi. Gliálne bunky, druhá zložka hematoencefalickej bariéry, priliehajú k vonkajšiemu povrchu kapilár. Vo vaskulárnych plexoch komôr mozgu je anatomickým základom bariéry epiteliálne bunky, ktoré sú taktiež pevne spojené. V súčasnej dobe je bariéra krv-mozog sa nepovažuje za anatomické a morfologické a funkčné ako formácia schopný selektívne prechádzať, a v niektorých prípadoch a dodaná do nervových buniek pomocou aktívnych transportných mechanizmov na rôzne molekuly. Preto bariéra vykonáva regulačné a ochranné funkcie
V mozgu sú štruktúry, v ktorých je oslabená hematoencefalická bariéra. To predovšetkým, hypotalamus, rovnako ako celá rada útvarov v spodnej časti 3. A 4. Komôr - zadné okno (oblasť postrema), subfornical subkomissuralny a orgánov, ako aj epifýza. Integrita BBB je narušená ischemickými a zápalovými léziami mozgu.
Krvno-mozgová bariéra sa považuje za konečne vytvorenú, keď vlastnosti týchto buniek spĺňajú dve podmienky. Po prvé, miera endocytózy v kvapalnej fáze (pinocytóza) v nich by mala byť extrémne nízka. Po druhé, musia sa vytvoriť špecifické husté kontakty medzi bunkami, pre ktoré je charakteristický veľmi vysoký elektrický odpor. Dosahuje hodnoty 1000-3000 ohm / cm 2 pre kapilárne Pial a od roku 2000 do 8000 0m / cm2 po dobu intraparenchymatózních mozgových kapilár. Pre porovnanie: priemerná hodnota transendoteliálneho elektrického odporu kapilár skeletálneho svalu je iba 20 ohmov / cm2.
Priepustnosť hematoencefalickej bariéry pre väčšinu látok je do značnej miery determinovaná ich vlastnosťami, ako aj schopnosťou neurónov syntetizovať tieto látky samostatne. Medzi látky, ktoré môžu prekonať túto bariéru, patrí predovšetkým kyslík a oxid uhličitý, ako aj rôzne kovové ióny, glukóza, esenciálne aminokyseliny a mastné kyseliny potrebné pre normálne fungovanie mozgu. Preprava glukózy a vitamínov sa uskutočňuje pomocou vektorov. Súčasne má D- a L-glukóza rôznu mieru penetrácie cez bariéru - v prvom prípade je viac ako 100-krát vyššia. Glukóza hrá hlavnú úlohu pri energetickom metabolizme mozgu a pri syntéze mnohých aminokyselín a proteínov.
Hlavným faktorom, ktorý určuje fungovanie hematoencefalickej bariéry, je úroveň metabolizmu nervových buniek.
Neuróny sú vybavené potrebnými látkami nielen pomocou vhodných krvných kapilár, ale aj s procesmi mäkkých a arachnoidných škrupín, nad ktorými cirkuluje cerebrospinálna tekutina. Cerebrospinálna tekutina sa nachádza v dutine lebky, v komorách mozgu av priestoroch medzi membránami mozgu. U ľudí je jeho objem asi 100 až 150 ml. V dôsledku cerebrospinálnej tekutiny sa zachováva osmotická rovnováha nervových buniek a odstránia sa metabolické produkty toxické pre nervové tkanivo.
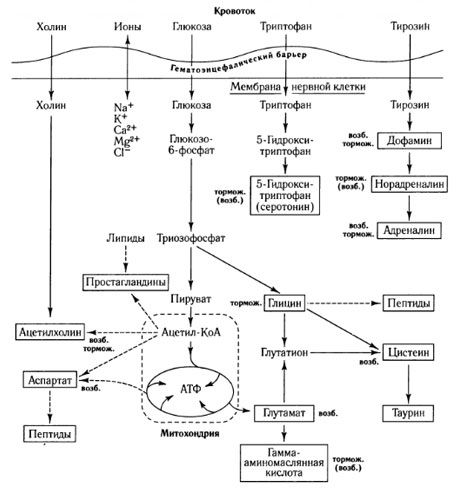
Spôsoby výmeny mediátorov a úloha hematoencefalickej bariéry v metabolizme (na: Shepherd, 1987)
Prechod látok cez hematoencefalickú bariéru závisí nielen od priepustnosti cievnej steny (molekulová hmotnosť, náboj a lipofilnosť látky), ale aj od prítomnosti alebo neprítomnosti aktívneho transportného systému.
Stereošpecifický inzulín-nezávislý glukózový transportér (GLUT-1), ktorý zabezpečuje prenos tejto látky cez hematoencefalickú bariéru, je bohatý na endotelové bunky kapilár mozgu. Aktivita tohto transportéra môže zabezpečiť dodávanie glukózy v množstve 2 až 3 krát vyšším, ako je mozog požadovaný za normálnych podmienok.
Charakteristika dopravných systémov hematoencefalickej bariéry (po: Pardridge, Oldendorf, 1977)
|
Prepojiteľné |
Primárny substrát |
Km, mM |
Vmax |
|
Hexózy |
Glukóza |
9 |
1600 |
|
Monokarboxylové |
Laktát |
1.9 |
120 |
|
Neutrálne |
Fenylalanín |
0.12 |
30 |
|
Základné |
Lyzín |
0.10 |
6 |
|
Vražda |
Zmiešať |
0.22 |
6 |
|
Purines |
Adenín |
0027 |
1 |
|
Nukleozidov |
Adenozín |
0018 |
0.7 |
U detí s narušením fungovania tohto transportéra dochádza k výraznému zníženiu hladiny glukózy v mozgovomiechovej moku a narušeniu vývoja a fungovania mozgu.
Monokarboxylové kyseliny (L-laktát, acetát, pyruvát), ako aj ketónové telieska sa prepravujú samostatnými stereošpecifickými systémami. Hoci intenzita ich transportu je nižšia ako transport glukózy, sú dôležitým metabolickým substrátom u novorodencov a na lačno.
Transport cholínu do centrálneho nervového systému je tiež sprostredkovaný nosičom a môže byť regulovaný rýchlosťou syntézy acetylcholínu v nervovom systéme.
Vitamíny nie sú syntetizované mozgom a sú dodávané z krvi pomocou špeciálnych dopravných systémov. Napriek skutočnosti, že tieto systémy majú relatívne nízku dopravnú aktivitu, za normálnych podmienok môžu zabezpečiť prepravu množstva vitamínov potrebných pre mozog, ale ich nedostatok v potravinách môže viesť k neurologickým poruchám. Niektoré plazmatické proteíny môžu tiež preniknúť cez hematoencefalickú bariéru. Jedným zo spôsobov ich penetrácie je transcytóza, sprostredkovaná receptormi. Takto preniká inzulín, transferín, vazopresín a rastový faktor podobný inzulínu bariére. Endotelové bunky kapilár mozgu majú špecifické receptory pre tieto proteíny a sú schopné uskutočňovať endocytózu komplexu proteín-receptor. Je dôležité, aby sa v dôsledku následných udalostí komplex rozpadol, intaktný proteín sa mohol uvoľniť na opačnej strane bunky a receptor sa opätovne vložil do membrány. Pre polykatiónové proteíny a lektíny je metódou penetrácie BBB tiež transcytóza, ale nie je spojená s pôsobením špecifických receptorov.
Veľa neurotransmiterov prítomných v krvi nie je schopných preniknúť do BBB. Dopamín teda nemá túto schopnosť, zatiaľ čo L-Dopa preniká cez BBB s použitím neutrálneho transportného systému aminokyselín. Okrem toho, kapilárne bunky obsahujú enzýmy metabolizujúcich neurotransmiterov (cholínesterázy, GABA-transaminázy aminopeptidázy et al.), Liečivá a toxických látok, ktorý poskytuje nielen ochranu mozgu z krvi cirkulujúcej neurotransmiterov, ale aj na toxíny.
GEB sa tiež podieľa na nosičových proteínoch, ktoré prenášajú látky z endotelových buniek kapilár mozgu do krvi a zabraňujú ich penetrácii do mozgu, napríklad b-glykoproteínu.
V priebehu ontogenézy sa výrazne mení rýchlosť dopravy rôznych látok prostredníctvom BBB. Preto rýchlosť transportu b-hydroxybutyrátu, tryptofánu, adenínu, cholínu a glukózy u novorodencov je významne vyššia ako u dospelých. To odzrkadľuje pomerne vyššiu potrebu vývoja mozgu v energetických a makromolekulárnych substrátoch.


 [
[