Lekársky expert článku
Nové publikácie
Kryptokoková meningitída
Posledná kontrola: 12.07.2025

Všetok obsah iLive je lekársky kontrolovaný alebo kontrolovaný, aby sa zabezpečila čo najväčšia presnosť faktov.
Máme prísne smernice týkajúce sa získavania zdrojov a len odkaz na seriózne mediálne stránky, akademické výskumné inštitúcie a vždy, keď je to možné, na lekársky partnerské štúdie. Všimnite si, že čísla v zátvorkách ([1], [2] atď.) Sú odkazmi na kliknutia na tieto štúdie.
Ak máte pocit, že niektorý z našich obsahov je nepresný, neaktuálny alebo inak sporný, vyberte ho a stlačte kláves Ctrl + Enter.
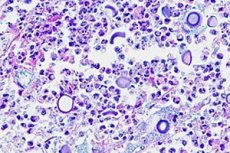
Zápal mozgových blán môže byť spôsobený nielen baktériami, vírusmi a protistami, ale aj plesňovými infekciami. Kryptokoková meningitída je spôsobená enkapsulovanými kvasinkovými hubami Cryptococcus neoformans, čo je oportúnny patogén u ľudí. [ 1 ] Bola pomenovaná Busse-Buschkeho choroba podľa jej prvého opisu Ottom Bussem a Abrahamom Buschkem v roku 1894. [ 2 ]
Podľa ICD-10 je kód ochorenia G02.1 (v časti o zápalových ochoreniach centrálneho nervového systému) a tiež B45.1 v časti o mykózach (t. j. plesňových ochoreniach).
Epidemiológia
Osem z desiatich prípadov kryptokokovej meningitídy sa vyskytuje u ľudí infikovaných HIV/AIDS.
Podľa údajov publikovaných v časopise The Lancet Infectious Diseases na jar 2017 táto huba spôsobuje každý rok približne 220 000 prípadov kryptokokovej meningitídy u ľudí s HIV alebo AIDS a viac ako 180 000 z nich zomrie. Väčšina prípadov kryptokokovej meningitídy sa vyskytuje v subsaharskej Afrike.
Podľa štatistík WHO bolo v roku 2017 v Afrike zaregistrovaných 165,8 tisíc prípadov kryptokokovej meningitídy, v ázijských krajinách 43,2 tisíc, v Severnej a Južnej Amerike 9,7 tisíc a v európskych krajinách 4,4 tisíc prípadov ochorenia.
Príčiny kryptokoková meningitída
Príčiny tohto typu meningitídy sú infekcia hubou Cryptococcus neoformans (trieda Tremellomycetes, rod Filobasidiella), ktorá žije v prostredí: v pôde (vrátane prachu), na hnijúcom dreve, v truse vtákov (holuby) a netopierov atď. K infekcii dochádza vzduchom - vdýchnutím aerosólových bazidiospór huby, hoci u väčšiny ľudí s dostatočnou imunitou k rozvoju ochorenia C. neoformans nevedie a zostáva fakultatívnym intracelulárnym oportúnnym mikroorganizmom (ktorý nemôže infikovať iných ľudí). Prečítajte si tiež - Kryptokoky - pôvodcovia kryptokokózy [ 3 ]
Kryptokoková meningitída sa spravidla vyvíja u HIV-infikovaných jedincov (v štádiu IVB) – ako sekundárna infekcia, ako aj u ľudí so zle fungujúcim imunitným systémom pri iných ochoreniach sprevádzaných dlhodobou imunosupresiou. [ 4 ]
Kryptokoková meningitída sa považuje za mozgovú alebo extrapulmonálnu formu kryptokokózy, ktorá sa vyvíja po hematogénnom šírení C. neoformans z dýchacích ciest a pľúc do mozgu a miechy.[ 5 ]
Rizikové faktory
Medzi faktory, ktoré zvyšujú riziko vzniku kryptokokovej meningitídy, patria:
- novorodenecké obdobie (obdobie novorodenca) a predčasný pôrod dojčiat;
- oslabenie imunitného systému pri onkologických ochoreniach (vrátane leukémie, mnohopočetného melanómu, lymfosarkómu), u pacientov s HIV infekciou a AIDS;
- cukrovka;
- vírusová hepatitída a iné ochorenia imunitných komplexov;
- kosáčikovitá anémia;
- chemoterapia v prítomnosti onkologickej diagnózy;
- prekročenie prípustnej úrovne ionizujúceho žiarenia;
- dlhé kúry antibiotickej alebo steroidnej liečby;
- inštalácia intravaskulárnych katétrov a shuntov;
- transplantácia kostnej drene alebo vnútorných orgánov.
Patogenézy
Kryptokoky, chránené pred ľudskými imunitnými bunkami polysacharidovou kapsulou (ktorá inhibuje fagocytózu), vylučujú proteázy, ureázu, fosfolipázu a nukleázu – enzýmy schopné ničiť hostiteľské bunky. [ 6 ]
A patogenéza kryptokokózy spočíva v tom, že tieto enzýmy poškodzujú bunky lýzou membrán, modifikujú molekuly, narúšajú funkcie bunkových organel a menia cytoskelet. [ 7 ]
Plesňové serínové proteázy ničia peptidové väzby bunkových proteínov, štiepia imunoglobulíny a proteíny imunitných efektorových buniek a replikácia C. neoformans prebieha v mononukleárnych fagocytoch (makrofágoch), čo uľahčuje ich šírenie. [ 8 ]
Okrem toho, prechodom cez endotelové bunky a prenosom vo vnútri infikovaných makrofágov kryptokoky narúšajú integritu hematoencefalickej bariéry (HEB). Huba sa šíri krvným obehom do mozgovomiechového moku a potom do mäkkých membrán mozgu, pričom v mozgovom tkanive vytvára „kolónie“ hubových buniek vo forme želatínových pseudocýst. [ 9 ]
Príznaky kryptokoková meningitída
Prvými príznakmi kryptokokovej meningitídy sú horúčka (teplota stúpa na +38,5-39°C) a silné bolesti hlavy.
Medzi klinické príznaky patrí aj nevoľnosť a vracanie, záchvaty, stuhnutosť krku, zvýšená citlivosť očí na svetlo a poruchy vedomia a správania. [ 10 ]
Ako poznamenávajú odborníci, vývoj meningeálneho syndrómu je pomalší ako pri bakteriálnej infekcii mozgových blán.
Komplikácie a následky
Komplikácie a následky plesňovej meningitídy spôsobenej kryptokokom sú:
- významné zvýšenie intrakraniálneho tlaku;
- izolované poškodenie hlavových nervov s parézou/paralýzou tvárového nervu a atrofickými zmenami zrakového nervu (vedúcimi k oftalmologickým problémom);
- šírenie zápalového procesu do tkanív subkortexu a hemisfér mozgu - kryptokoková meningoencefalitída;
- vývoj mozgového abscesu (kryptokokómu);
- výpotok do subdurálneho priestoru (pod tvrdou mozgovou membránou);
- poranenie miechy;
- mentálne zmeny a znížené kognitívne funkcie.
Diagnostika kryptokoková meningitída
Okrem anamnézy a fyzikálneho vyšetrenia zahŕňa diagnostika infekcie C. neoformans pri meningitíde nevyhnutne krvné testy: všeobecné klinické a biochemické, analýzu krvného séra na protilátky proti proteínom C. neoformans a hemokultúru.
Vykoná sa lumbálna punkcia aanalýza mozgovomiechového moku na antigén a bakterioskopická analýza (bakteriálna kultúra) mozgovomiechového moku. [ 11 ]
Inštrumentálna diagnostika sa vykonáva pomocou röntgenového vyšetrenia hrudníka a magnetickej rezonancie mozgu.
Odlišná diagnóza
Diferenciálna diagnostika zahŕňa meningitídu a meningoencefalitídu bakteriálnej a vírusovej etiológie, poškodenie mozgu hubami Histoplasma capsulatum, Coccidioides immitis, Blastomyces dermatitidis alebo amébami (vrátane Naegleria fowleri).
Liečba kryptokoková meningitída
Etiologická liečba je zameraná na eradikáciu kryptokokov, na čo sa používajú antimykotiká.
Liečebný režim zahŕňa intravenózne podanie (kvapkaním, cez centrálny venózny katéter alebo peritoneálnou infúziou) polyénového antifungálneho antibiotika Amfotericín B (Amphocyl) v kombinácii s antifungálnym liekom Flucytozín (5-fluórcytozín) alebo Flukonazol, ktorý má fungicídny a fungistatický účinok. Dávkovanie týchto liekov sa vypočíta v závislosti od telesnej hmotnosti pacienta.
Je potrebné neustále monitorovať stav pacienta, pretože amfotericín B má toxický účinok na obličky a vedľajšie účinky flucytozínu môžu zahŕňať potlačenie hematopoetickej funkcie kostnej drene, zástavu dýchania alebo srdca, rozvoj kožných lézií vo forme epidermálnej nekrolýzy atď.
Podľa odporúčaní publikovaných v aktualizácii IDSA (Infectious Diseases Society of America) z roku 2010 sa liečba nezmenila desať rokov. Antifungálna liečba prvej línie je založená na indukcii, konsolidácii a udržiavaní liečby u nasledujúcich troch typov pacientov: [ 12 ]
Choroby súvisiace s HIV
- Indukčná terapia
- Amfotericín B deoxycholát (0,7 – 1,0 mg/kg/deň) + flucytozín (100 mg/kg/deň perorálne) počas 2 týždňov (dôkaz A1)
- Lipozomálny amfotericín B (3 – 4 mg/kg/deň) alebo lipidový komplex amfotericín B (5 mg/kg/deň; monitorovať funkciu obličiek) + flucytozín (100 mg/kg/deň) počas 2 týždňov (dôkaz B2)
- Amfotericín B deoxycholát (0,7 až 1,0 mg/kg/deň) alebo lipozomálny amfotericín B (3 až 4 mg/kg/deň) alebo lipidový komplex amfotericínu B (5 mg/kg/deň u pacientov, ktorí netolerujú flucytozín) počas 4 až 6 týždňov (dôkaz B2)
- Alternatívy k indukčnej terapii
- Amfotericín B deoxycholát + flukonazol (Dôkaz B1)
- Flukonazol + flucytozín (dôkaz B2)
- Flukonazol (dôkaz B2)
- Itrakonazol (dôkaz C2)
- Flukonazol (400 mg/deň) počas 8 týždňov (údaje A1)
- Flukonazol (200 mg/deň) počas 1 alebo viacerých rokov (dôkaz A1)
- Itrakonazol (400 mg/deň) počas 1 alebo viacerých rokov (dôkaz C1)
- Amfotericín B deoxycholát (1 mg/kg/týždeň) počas 1 alebo viacerých rokov (dôkaz C1)
- Konsolidačná terapia
- Podporná terapia
- Alternatívy k udržiavacej terapii
Choroby súvisiace s transplantáciou
- Indukčná terapia
- Lipozomálny amfotericín B (3 – 4 mg/kg/deň) alebo lipidový komplex amfotericín B (5 mg/kg/deň) + flucytozín (100 mg/kg/deň) počas 2 týždňov (dôkaz B3)
- Alternatívy k indukčnej terapii
- Lipozomálny amfotericín B (6 mg/kg/deň) alebo lipidový komplex amfotericín B (5 mg/kg/deň) počas 4 – 6 týždňov (dôkaz B3)
- Amfotericín B deoxycholát (0,7 mg/kg/deň) počas 4 – 6 týždňov (dôkaz B3)
- Flukonazol (400 až 800 mg/deň) počas 8 týždňov (dôkaz B3)
- Flukonazol (200 až 400 mg/deň) počas 6 mesiacov až 1 roka (dôkaz B3)
- Konsolidačná terapia
- Podporná terapia
Ochorenie nesúvisiace s HIV/transplantáciou
- Indukčná terapia
- Amfotericín B deoxycholát (0,7 až 1,0 mg/kg/deň) + flucytozín (100 mg/kg/deň) počas 4 alebo viacerých týždňov (dôkaz B2)
- Amfotericín B deoxycholát (0,7 – 1,0 mg/kg/deň) počas 6 týždňov (dôkaz B2)
- Lipozomálny amfotericín B (3 – 4 mg/kg/deň) alebo lipidový komplex amfotericín B (5 mg/kg/deň) v kombinácii s flucytozínom, 4 týždne (dôkaz B3)
- Amfotericín B deoxycholát (0,7 mg/kg/deň) + flucytozín (100 mg/kg/deň) počas 2 týždňov (dôkaz B2)
- Konsolidačná terapia
- Flukonazol (400 až 800 mg/deň) počas 8 týždňov (dôkaz B3)
- Flukonazol (200 mg/deň) počas 6 – 12 mesiacov (dôkaz B3)
- Podporná terapia
Kombinácia amfotericínu B a flucytozínu sa ukázala ako najúčinnejšia pri eliminácii infekcie a preukázala väčší prínos pre prežitie ako samotný amfotericín. Avšak kvôli svojej cene je flucytozín často nedostupný v prostrediach s obmedzenými zdrojmi a vysokou mierou výskytu ochorenia. Kombinácie amfotericínu B a flukonazolu boli študované a preukázali lepšie výsledky v porovnaní so samotným amfotericínom B.[ 13 ], [ 14 ], [ 15 ]
Bez liečby klinický priebeh progreduje do zmätenosti, záchvatov, zníženej úrovne vedomia a kómy.
Bolesť hlavy refraktérna na analgetiká sa môže liečiť spinálnou dekompresiou po adekvátnom neurozobrazovacom vyšetrení pomocou CT alebo MRI. Bezpečný maximálny objem mozgovomiechového moku, ktorý je možné odobrať jednou lumbálnou punkciou, nie je jasný, ale často sa odoberie až 30 ml s kontrolou tlaku po každých odobratých 10 ml.[ 16 ]
Prevencia
Prevencia infekcie hubou Cryptococcus neoformans je nevyhnutná predovšetkým v prípadoch oslabeného imunitného systému. [ 17 ] Odporúča sa vyhýbať sa prašným miestam a práci s pôdou a ľudia infikovaní HIV by mali dostávať priebežnú antiretrovírusovú liečbu.
Predpoveď
Bez liečby je prognóza akejkoľvek plesňovej meningitídy zlá.
Počiatočná prognóza závisí od prediktorov úmrtnosti, ako sú nasledujúce [ 18 ], [ 19 ]:
- Otvárací tlak mozgovomiechového moku je vyšší ako 25 cm H2O.
- Nízky počet bielych krviniek v mozgovomiechovom moku
- Senzorické poškodenie
- Neskorá diagnóza
- Zvýšené titre antigénov v mozgovomiechovom moku
- Miera odstránenia infekcie
- Množstvo kvasiniek v mozgovomiechovom moku presahuje 10 mm3 ( bežná prax v Brazílii) [ 20 ]
- Pacienti bez HIV a prognostické faktory u týchto pacientov, okrem už uvedených:
- Markery slabej zápalovej reakcie
- Žiadne bolesti hlavy
- Primárna hematologická malignita
- Chronické ochorenie obličiek alebo pečene
Úmrtnosť sa v jednotlivých krajinách líši v závislosti od dostupných zdrojov. V Spojených štátoch a Francúzsku zostáva vysoká, pričom úmrtnosť do 10 týždňov sa pohybuje od 15 % do 26 % a u pacientov bez infekcie HIV je ešte vyššia v dôsledku neskorej diagnózy a dysfunkčných imunitných odpovedí. Na druhej strane, v krajinách s nízkymi zdrojmi sa úmrtnosť v 10. týždni zvyšuje z 30 % na 70 % v dôsledku neskorej prezentácie ochorenia a nedostatočného prístupu k liekom, monitorom krvného tlaku a optimálnemu monitorovaniu.

